
Buğday hastalık modelleri
Buğday patlaması
Patojen
Pyricularia griseaolarak da bilinir. Magnaporthe oryzaebuğday bitkilerini etkileyen önemli bir hastalık olan buğday patlamasından sorumlu bir mantar patojenidir. Patojen öncelikle enfeksiyonları başlatmak için birincil inokulum görevi gören konidiler (eşeysiz sporlar) yoluyla eşeysiz olarak çoğalır. Bu konidiler konidiyoforlar üzerinde üretilir ve rüzgar, yağmur ve tarım ekipmanları gibi mekanik yollarla dağılır. Duyarlı bir buğday konukçusuna konduktan sonra, konidiler çimlenir ve bitki dokusuna nüfuz etmeyi kolaylaştıran özelleşmiş yapılar olan appressoria oluşturur. Mantar içeri girdikten sonra konakçı hücreleri kolonize ederek hastalık gelişimine yol açar. Çevresel koşullar, buğdayın enfeksiyon sürecinde çok önemli bir rol oynar. P. grisea. Fungus, 15°C ila 30°C arasında değişen sıcaklıklar ve uzun süreli yaprak ıslaklığı veya yüksek bağıl nem ile sıcak ve nemli iklimlerde gelişir. Enfeksiyonu başlatmak için en az 14 saat boyunca sürekli yaprak ıslaklığı gereklidir, bu da aşırı bulut örtüsü, yüksek nem, aşırı sulama ve yanlış zamanlanmış sulamayı hastalık gelişimine elverişli hale getirir. Ayrıca kuraklık, toprak sıkışması, düşük biçme yükseklikleri ve aşırı azot gübrelemesi gibi stres faktörleri hastalığın şiddetini artırabilir.
Semptomlar
Buğday yanıklığının ilk belirtileri yapraklarda suyla ıslanmış, baklava şeklinde lezyonlar olarak ortaya çıkar ve hastalık ilerledikçe bu lezyonlar griye döner. Bu lezyonlar genişleyebilir ve birleşerek geniş yaprak yanıklığı ve nekroza yol açabilir. Enfekte başaklar, genellikle rachis veya başakların tabanındaki siyahımsı-gri bir enfeksiyon noktasından başlayarak kısmen veya tamamen ağarma gösterir. Yüksek inokulum baskısı altında, tek bir rachis üzerinde birden fazla enfeksiyon noktası oluşabilir ve bu da önemli verim kayıplarına neden olur. Yaprak semptomlarına ek olarak, P. grisea düğümler ve boyunlar da dahil olmak üzere buğday bitkisinin diğer toprak üstü kısımlarını enfekte ederek çürük boyun veya düğüm patlamasına yol açabilir. Bu durum etkilenen kısımların kırılmasına neden olarak yatmaya ve verimin daha da düşmesine yol açabilir. Patojenin büyüme mevsimi boyunca bitkinin çeşitli kısımlarını enfekte etme yeteneği, özellikle uygun çevresel koşullar altında onu özellikle yıkıcı hale getirir.
FieldClimate modeli
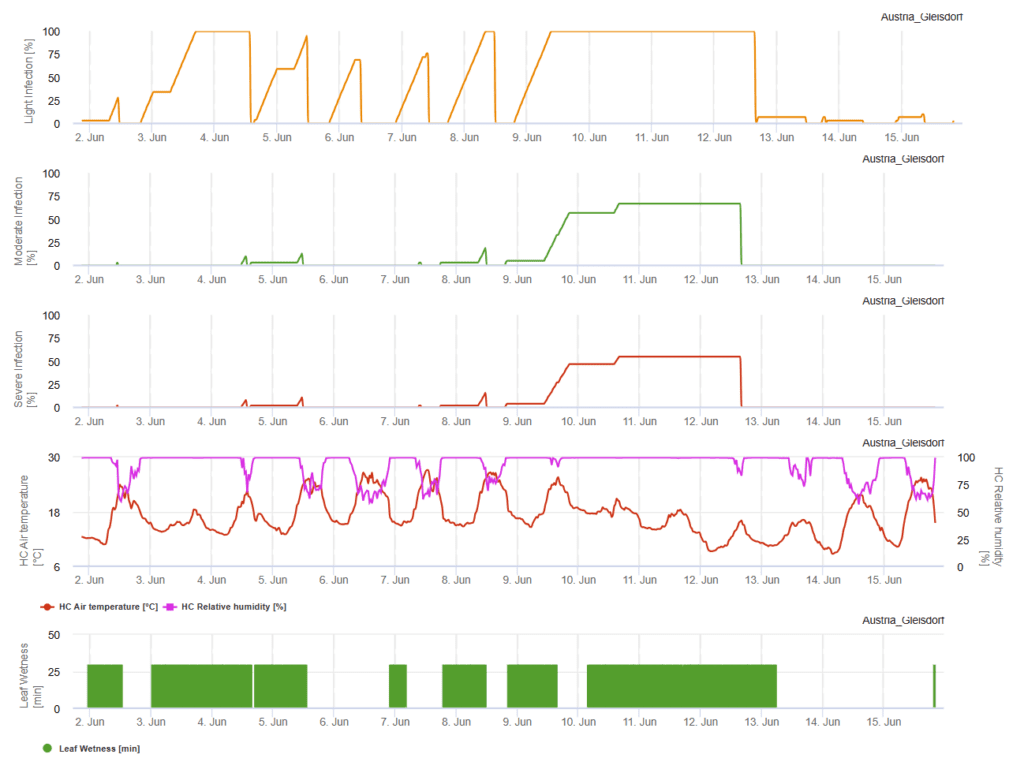
Sensörlere ihtiyaç var:
- Hava Sıcaklığı
- Bağıl Nem
- Yaprak Islaklığı
Bulutlu gökyüzü, nemli koşullar ve çiseleyen yağmurlar hastalığın gelişimini ve şiddetini desteklemektedir. FieldClimate'de üç şiddet sınıfı hesaplanır ve enfeksiyonun 100%'sine ulaşıldığında fungal patojen için tarlada en uygun koşullar sağlanmış olur. Çeşitliliğe bağlı olarak, hafif, orta veya şiddetli bir enfeksiyon 100%'ye ulaştığında tarla geçmişi iyileştirici bitki koruma önlemleri dikkate alınmalıdır.
Edebiyat
- Cruz, C. D., & Valent, B. (2017). Buğday patlaması hastalığı: hareket halindeki tehlike. Tropikal Bitki Patolojisi, 42(3), 210-222.
- Islam, M. T., Croll, D., Gladieux, P., Soanes, D. M., Persoons, A., Bhattacharjee, P., ... & Talbot, N. J. (2016). Bangladeş'te buğday patlamasının ortaya çıkmasına Magnaporthe oryzae'nin Güney Amerika soyu neden oldu. BMC Biyoloji, 14(1), 84.
Pyrenophora teres
Patojen
Pyrenophora teres (Drechslera teres) iki şekilde bulunur - P. teres f. teres ve P. teres f. maculata Bu da sırasıyla ağ şeklinde ağ lekesi ve nokta şeklinde ağ lekesine neden olur.
Pseudothecia'dan salınan askosporlar kalıntıları enfekte ederek birincil enfeksiyonu başlatır. Tohum kaynaklı misel ve konidiler de bazı durumlarda birincil inokulum görevi görür. Sporlar yapraklarda çimlenir ve dış epidermal hücre duvarına nüfuz eder, böylece patojen büyük bir hücre içi vezikül içinde gelişebilir. Bunu, konidilerin üretildiği ve ikincil enfeksiyonu tetikleyerek hastalığın şiddetini artıran aseksüel aşama izler. Büyüme mevsiminin sonunda, patojen aşırı mevsim kaynağı olarak psödotesyum üretir ve bunlar enfekte arpa döküntüleri üzerinde kalır.
Semptomlar
Belirtiler yapraklarda, gövdelerde ve çekirdeklerde ortaya çıkar ve hastalık bitkilerin altından üstüne doğru ilerler. Daha yaşlı bitkiler, patojen penetrasyonunu önleyen daha kalın bir kütikül ve antifungal bileşikler üretme kabiliyetine sahip oldukları için daha az ciddi hasar görme eğilimindedir. Patojenler, nekroz ve kloroza katkıda bulunarak veya hücresel düzeyde su dengesini bozarak semptomlardan sorumlu olan toksinler üretir.
Ağ tipi leke hastalığı durumunda, belirtiler dar, koyu kahverengi, uzunlamasına lezyonlar şeklinde görülür. Oldukça dayanıklı çeşitlerde sadece birkaç küçük nokta benzeri lezyon gelişir ve belirgin bir ağ benzeri desen oluşumu görülmez. Buna karşın, çoğu duyarlı çeşitte nekrotik lezyonları çevreleyen klorotik veya suyla ıslanmış alanlar görülebilir.
Leke tipi leke için, semptomlar koyu kahverengi, dairesel veya eliptik lezyonlardan oluşur ve bunlar genellikle değişen genişlikte klorotik veya nekrotik bir hale ile çevrelenir. Daha az duyarlı çeşitlerde lezyonlar genellikle daha küçüktür ve çevreleyen klorotik bir haleden yoksun olabilir.
Şiddetli enfeksiyonlar yaprakların tamamen ölmesine ve kuru görünmesine neden olabilir. Tipik olarak önce yaşlı yapraklar, ardından da genç yapraklar solgunluk gösterir.
FieldClimate modeli
Drechslera teres Model
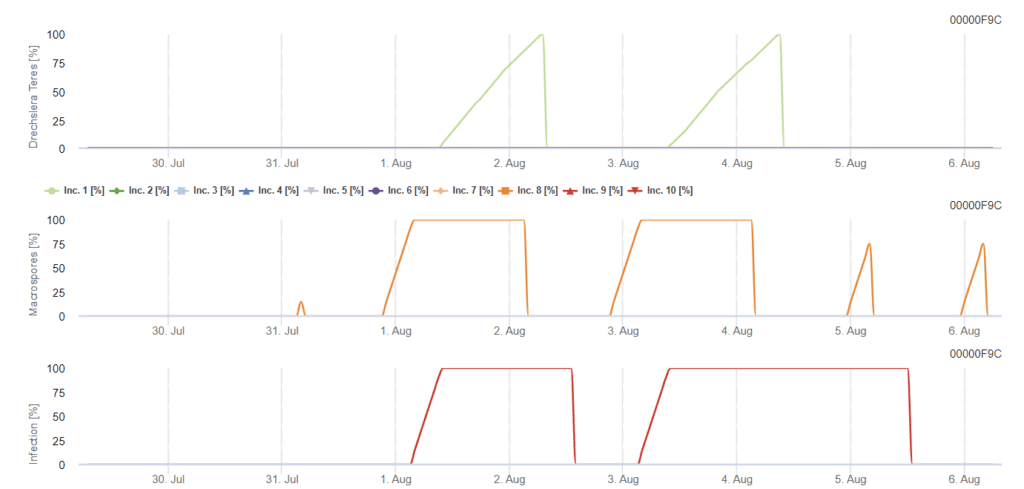
Sensörlere ihtiyaç var:
- Hava Sıcaklığı
- Bağıl Nem
- Yaprak Islaklığı
- Yağış
Birincil inokulum, optimum 20°C olmak üzere 15°C ile 25°C arasındaki optimum sıcaklıklarda gelişir. 6 saatin üzerindeki karanlık koşullar, konidi sporülasyon grafiğinde gösterildiği gibi konidilerin optimum büyümesine yol açar. Sporülasyon grafiği 100%'ye ulaşırsa, sahada optimum koşullar belirlenmiş demektir.
Daha fazla dağılma rüzgar veya yağmur yoluyla gerçekleşir. Bitki dokularının enfeksiyonları, enfeksiyon grafiğinde gösterildiği gibi, 15°C ve 25°C'lik optimum sıcaklıklarla yaklaşık 10 ila 30 saat boyunca yaprak ıslaklığı veya yüksek bağıl nem gibi nemli koşullara ihtiyaç duyar. 100%'ye ulaştığında, sahadaki enfeksiyon için en uygun koşulların ölçüldüğü belirlenir. Güneş ışığı, yüksek güneş radyasyonu ve düşük bağıl nem ile nemli ve kuru dönemlerin değişen koşullarını takiben konidia üreten konidoforların büyümesini de artırabilir ve rüzgar hastalık gelişimini destekler.
Edebiyat
- Backes, A., Guerriero, G., Ait Barka, E., & Jacquard, C. (2021). Pyrenophora teres: taksonomi, morfoloji, arpa ile etkileşim ve kontrol şekli. Bitki biliminde sınırlar, 12, 614951.
- Liu, Z., Ellwood, S. R., Oliver, R. P., & Friesen, T. L. (2011). Pyrenophora teres: giderek daha fazla zarar veren bir arpa patojeninin profili. Moleküler bitki patolojisi, 12(1), 1-19.
- Obst, A., & Paul, VH (1993). Tahıl hastalıkları ve zararlıları, Verlag Th. Mann, Gelsenkirchen-Buer.
Hepsini al
Patojen
'Take-all' hastalığına neden olan Gaeumannomyces graministahıllarda görülen en yıkıcı hastalıklardan biridir. Hastalığın hasat edecek tahıl bırakmayacak kadar zarar verici olması nedeniyle bu isim Güney Avustralyalı çiftçiler tarafından verilmiştir. Patojen kök sistemine ve gövdeye zarar vererek su ve besin eksikliğine neden olur ve sonunda bitkinin ölümüne yol açar.
Fungus, saprofit olarak bitki döküntülerinde misel olarak hayatta kalır ve toprak kaynaklı parçalar rüzgar, su ve hayvanlar tarafından taşınabilir. Birincil enfeksiyon, fidelerin kökleri enfekte olmuş döküntülerle temas ettiğinde meydana gelir, bunu hif büyümesi ve uzaması izler. Kök epidermisine nüfuz ederek ve kök korteksini istila ederek dokuları kolonize eder ve tahrip eder. Enfeksiyon yukarı ve aşağı doğru ilerler. İkincil enfeksiyon kökten köke temas yoluyla gerçekleşir ve ciddi şekilde enfekte olmuş bitkiler yamalar halinde görülür.
Semptomlar
Buğdayda tümünü alma hastalığı tipik olarak fide ve kardeşlenme aşamalarında etkili olur ve toprak yüzeyine yakın semptomlara neden olur. Enfekte olmuş bitkiler bodurlaşabilir, sararmış yapraklar ve tam gelişmiş tanelerden yoksun erken olgunlaşan başaklar görülebilir. Birkaç santimetreden metrelere kadar değişen dairesel ölü lekeler genellikle sarı-turuncu veya bronz kenarlara sahiptir ve sonraki yıllarda aynı alanda tekrar ortaya çıkabilir.
Temel belirtiler arasında ağarmış beyaz veya boş başaklar, kararmış gövde tabanları ve genişleyen küçük siyah lezyonlarla koyu, çürüyen kökler bulunur. Ciddi hasar görmüş kökler kırılgandır ve taban gövdesinde parlak siyah bir renk değişikliği görülebilir. Bitkiler zayıflamış kök sistemleri nedeniyle topraktan kolayca çıkarılabilir. Hastalık, bitkinin üst kısımlarına su akışını bozarak erken yanmaya neden olduğu için kuraklık stresine benzeyebilir.
FieldClimate modeli
Hepsini al
Model Sensörler:
- Toprak sıcaklığı
Take-all risk modeli, riskli dönemleri belirlemek için gün uzunluğu ve toprak sıcaklığını kullanır. Güneş ışığının 13 saatten az olduğu günler ve 10°C ile 20°C arasındaki toprak sıcaklıkları hastalık gelişimini desteklemektedir.
Risk değeri 100%'ye ulaştığında, tarlada patojen gelişimi için en uygun koşullar sağlanmış demektir. Duyarlı tahıllar arasında en az 2 ila 3 yıl aralıklarla ürün rotasyonu en önemli koruma stratejisidir.
Edebiyat
- Cook, R. J. (2003). Buğdayın hepsini al. Fizyolojik ve Moleküler Bitki Patolojisi, 62(2), 73-86.
- Palma-Guerrero, J., Chancellor, T., Spong, J., Canning, G., Hammond, J., McMillan, V. E., & Hammond-Kosack, K. E. (2021). Take-all hastalığı: önemli bir buğday kök patojenine ilişkin yeni bilgiler. Bitki Biliminde Eğilimler, 26(8), 836-848. https://www.apsnet.org/edcenter/disandpath/fungalasco/pdlessons/Pages/Takeall.aspx
Fusarium baş yanıklığı
Patojen
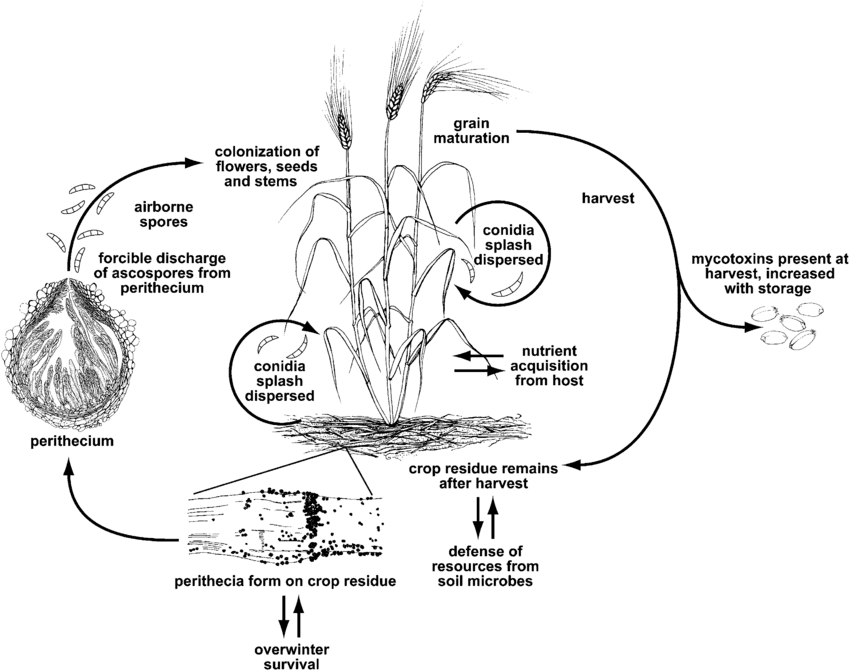
Fusarium baş yanıklığına veya kabuklanmaya şu cinsler neden olur Fusarium. En yaygın tür şudur Fusarium graminearum ancak en yaygın türler bölgelere göre farklılık gösterebilir.
F. graminearum buğday bitkilerini herhangi bir büyüme aşamasında enfekte edebilir. Kışı enfekte olmuş mahsul kalıntıları üzerinde geçirir ve ilkbaharda, perithecia ve konidialardan ascosporlar buğday glumes veya anthers üzerine dağıldığında birincil enfeksiyon meydana gelir. Enfekte olmuş çiçekler, genellikle "mezar taşı" taneleri olarak adlandırılan büzülmüş veya solmuş taneler üretir. Taneler etkilenmemiş gibi görünse bile mikotoksinlerle kontamine olabilirler. İkincil enfeksiyon konidiler yoluyla gerçekleşir, ancak buğday salgınları ikincil kaynaklardan ziyade birincil inokulum miktarına bağlıdır.
Fusarium baş yanıklığı ayrıca ürünlerde zararlı mikotoksin birikimine yol açarak hayvanlar için potansiyel bir risk oluşturur. Bu mikotoksinler bitkinin savunma mekanizmasını devre dışı bırakır veya mantarı diğer organizmalara karşı korur. Başlıca toksin deoksinivalenoldür (DON) ve protein sentezini inhibe ederek normal hücre fonksiyonunu bozar. DON'lu buğday tüketen insanlarda mide bulantısı, ateş veya kusma gibi semptomlar görülebilir.
Semptomlar

Buğday ve makarnalık buğdayda, başağın herhangi bir kısmı veya tamamı ağarmış görünebilir. Kısmen beyaz ve yeşil başaklar buğdaydaki hastalık için tanı koydurucudur. Fungus sapı da enfekte ederek kahverengi ila mor renk değişimine neden olabilir. Islak koşullarda enfekte başakçık ve başakçıklarda pembe ila somon turuncusu spor kitleleri sıklıkla görülür. Birçok çekirdek buruşuk ve hafiftir ve kireçli, cansız görünümleri nedeniyle bazen "mezar taşı" olarak adlandırılırlar. Uygun koşullar altında, enfeksiyon bitişik başakçıklara yayılabilir ve rachis ve peduncle dahil olmak üzere tüm başakçığı enfekte edebilir. Enfeksiyon gelişim evresinin sonlarında ortaya çıktığında, taneler normal boyutta donuk bir görünüme ve pembe renk değişimine sahip olabilir.
Arpada, enfekte başakçıklar ağarır ve suyla ıslanmış bir görünüm sergiler. Çekirdekler de renk değişikliği gösterebilir ve bazen ıslak koşullar sırasında başakçık ve glumes üzerinde somon-turuncu spor kütleleri görülebilir.
FieldClimate modelleri
Bir tarladaki FHB seviyelerine ilişkin tahminler, yanık başakların veya tanelerin sayımına dayanmaktadır. Buğdayda FHB'nin şiddetini tahmin etmek için renkli görsel ölçek NDSU Extension Service'ten temin edilebilir (PP-1095 yayını): https://library.ndsu.edu/ir/bitstream/handle/10365/9187/PP1095_1998.pdf?sequence=1&isAllowed=y.
Fusarium Head Blight Enfeksiyon Modeli (Fusarium Head Blight Riski)
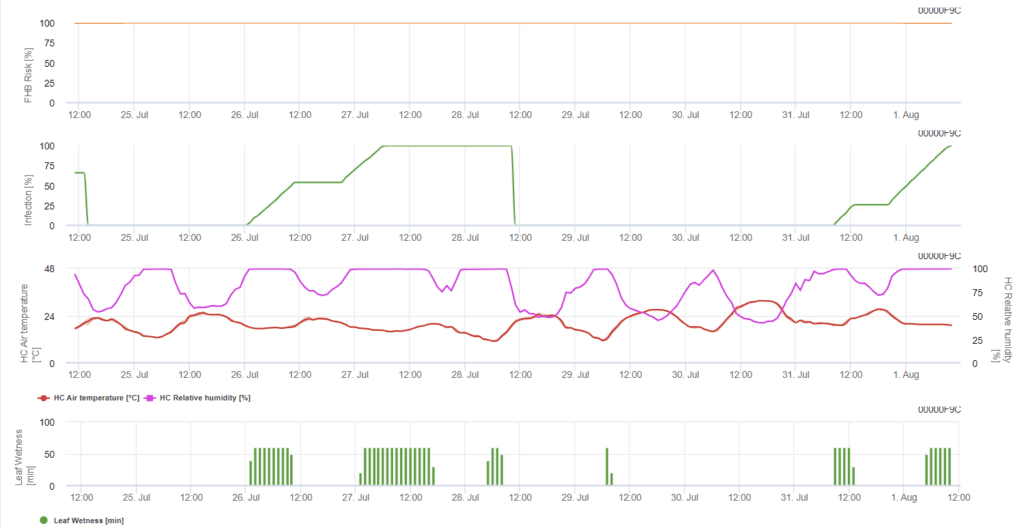
Sensörlere ihtiyaç var:
- Hava sıcaklığı
- Bağıl nem
- Yaprak ıslaklığı
Model, bir enfeksiyon için riskli dönemleri belirler. 100% enfeksiyonuna ulaşıldığında risk çok yüksektir ve fungus için koşullar enfeksiyon için elverişlidir. Çiftçinin farklı buğday çeşitlerinin gelişim aşaması hakkındaki bilgisi, enfeksiyondan hemen sonra iyileştirici bir sprey uygulamasına karar verme imkanı verir.
Buğdaydaki Fusarium Baş Yanıklığının mantar etkenleri, 20°C ila 30°C'lik ılık sıcaklıklar ve uzun nemli dönemler tarafından tercih edilir. Birkaç gün süren yaprak ıslaklık dönemleri erken görülebilir semptomlara yol açacaktır. Belirtiler, enfeksiyonu 18 saatlik veya daha kısa bir yaprak ıslaklık periyodu takip ederse ve 15°C sıcaklıklarda yapay bir aşılamadan sonra uzun bir gecikme döneminden sonra da görülebilir.
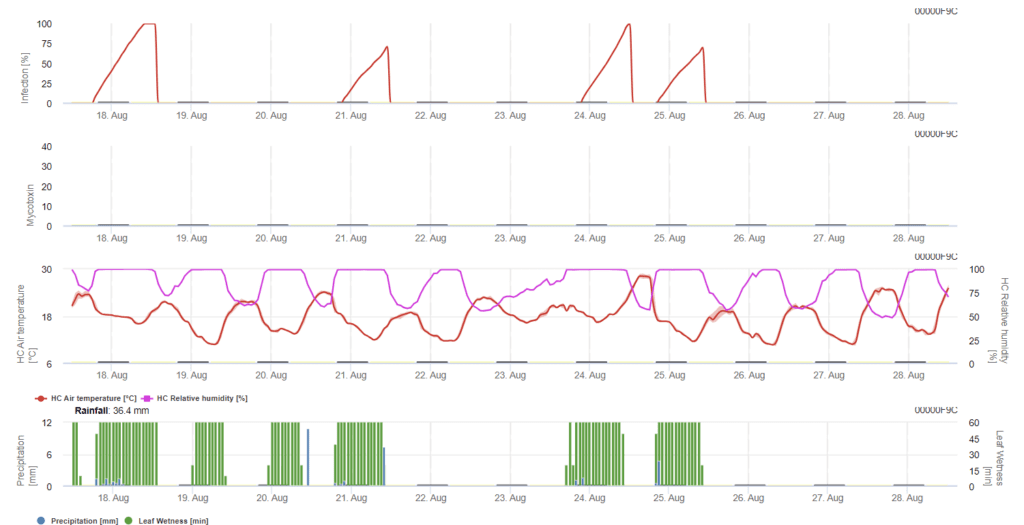
Literatürde bulduğumuz tüm farklı sıcaklık ve nem kombinasyonlarını özetleyerek, sıcaklık ve yaprak ıslaklık süresi veya 85%'den fazla bağıl neme sahip dönemler aşağıdaki grafikte görselleştirilen değerleri aşarsa Fusarium Baş Yanıklığı Enfeksiyonlarına işaret etmeye karar verdik. İlerleme değerinin hesaplanması, nemli koşulların süresi ile sıcaklık arasındaki ilişkiyi takip eder.
Fusarium Mikotoksin Uyarı Modeli (Fusarium Head Blight)
Sensörlere ihtiyaç var:
- Hava sıcaklığı
- Bağıl nem
- Yaprak ıslaklığı
- Yağış
Bu modelde FHB'nin enfeksiyonu yağış (2mm gerekli), bağıl nem (85%'nin üzerinde) veya yaprak ıslaklığı, işlem sırasındaki sıcaklık ile hesaplanır. Enfeksiyon 100%'ye ulaşırsa mantar patojeni için en uygun koşullara ulaşılmıştır. Model ayrıca FHB mikotoksin riskini de hesaplar.
Fusarium baş yanıklığının uzun yaprak ıslaklık süreleri ile yapılan enfeksiyon denemeleri yüksek mikotoksin içeriğine yol açmaktadır. Bu bilgiler ışığında, 61. ve 69. aşamalarda 48 saat veya daha fazla yaprak ıslaklık süresinin yüksek mikotoksin riski taşıdığı varsayılmaktadır.
Ticari olarak yetiştirilen buğdayda DON analizi boyunca elde edilen deneyimler, 61 ila 69. aşamalardaki ilk enfeksiyonu takiben enfeksiyon için yeterince uzun yaprak ıslaklık sürelerinin DON değerlerini artırabileceğini göstermiştir. Daha uzun yaprak ıslaklık süreleri durumunda mikotoksinler 85. aşamaya kadar artabilir.
- BBCH aşama 61: Çiçeklenme başlangıcı; ilk anterler görünür
- BBCH evre 69: Çiçeklenme sonu; tüm başakçıklar çiçeklenmeyi tamamlamıştır ancak bazı susuz kalmış anterler kalabilir
- BBCH aşaması 85: Olgunlaşmanın ortasında; tane içeriği yumuşak ama kuru, tırnak izi tutulmamış yumuşak hamur
Model, hesaplama için seçilen süre boyunca her başarılı enfeksiyon dönemi için enfeksiyon ilerlemesiyle orantılı risk rakamını biriktirir. Altı tamamlanmış enfeksiyon 100% riskine yol açacaktır. Normalde, bir fusarium enfeksiyonuna yol açan yaprak ıslaklık süresi, gereken minimum süreden daha uzundur. Bu nedenle, çoğu fusarium enfeksiyonu 17%'den daha fazla bir risk artışına yol açacaktır.
Mikotoksin risk değeri tarla geçmişine bağlıdır. Toprak işlemesiz buğdaydan sonra yetiştirilen buğday, optimum durumda ilaçlanmadığı takdirde sadece küçük bir risk taşıyabilir. İlaçlanmamış buğdayda, riskin 35%'sinden sonra DON değerlerinin artmasını beklemeliyiz. Başka bir ürünü takip eden toprak işlemesiz buğdaydan sonraki buğday 50%'lik daha yüksek bir risk taşıyabilir. Toprak işlemeli buğdaydan sonra buğdayımız varsa, risk 70%'ye kadar yükselebilir. Risk 100%'ye ulaşırsa ilk yıl buğdayı DON için test edilmelidir.
Edebiyat
- https://www.fao.org/4/y4011e/y4011e0j.htm
- https://scabusa.org/pdfs/NDSU_PP-804_FHB-Small-Grains.pdf
- Lancashire, P. D., Bleiholder, H., Boom, T. V. D., Langelüddeke, P., Stauss, R., Weber, E., & Witzenberger, A. (1991). Bitkilerin ve yabani otların büyüme aşamaları için tek tip bir ondalık kod. Annals of applied Biology, 119(3), 561-601.
- Trail, F. (2009). Yanık tahıl dalgaları için: Postgenomik çağda Fusarium graminearum. Bitki fizyolojisi, 149(1), 103-110.
- Schumann, G. L. (2010). Bitki Sağlığı Eğitmeni| Cilt: 10| Yıl: 2010| Makale Türü: Ders Planları. Bitki Sağlığı, 10.
Arpa şeridi
Patojen
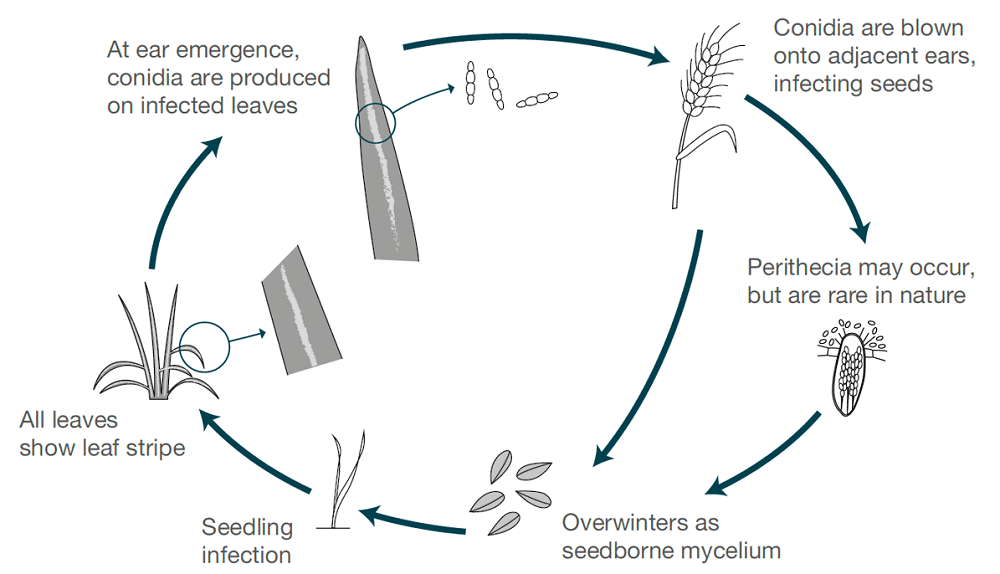
Arpa şeridine şunlar neden olur Pyrenophora graminea (Drechslera graminea)enfekte olmuş bir tohumun epidermisinde hayatta kalan tohum kaynaklı bir patojendir. Mantar, fideleri serin ve nemli koşullar altında enfekte eder. Mantar bitki içinde sistemik olarak büyür, tüm bitkiyi enfekte eder, toksin üretir, hücreleri öldürür ve damarlar arasındaki yaprak dokusunun rengini değiştirerek çizgili lezyonlara neden olur. Çizgili lezyonlar kışlık arpada ilkbahar arpasına göre daha yaygındır.
Koşullar ıslak veya nemli olduğunda, sağlıklı bitki başakları çiçek açtığında yaprak yüzeyinde sporlar üretilir. Sporlar rüzgarla bu gelişmekte olan başaklara dağılır, çimlenir ve enfeksiyonlara neden olur. Çekirdekler en çok erken gelişme döneminde duyarlıdır. Her sezon sadece bir enfeksiyon ve spor üretimi döngüsü gerçekleşir.
Semptomlar

Belirtiler en çok kulak çıkma aşamasında belirginleşir.
Başlangıçta yaprağın ve yaprak kınının taban kısmında soluk yeşil ila sarı çizgiler görülür. Bu çizgiler giderek kahverengiden koyu kahverengiye döner ve bunu yaprak ayasının kuruması ve yarılması izler. Boyutları yaprağın tüm uzunluğuna yayılır, nekrotik hale gelir ve birleşerek sonunda bitkinin ölümüne yol açar.
Bitkiler bodur görünebilir, az sayıda tiller üretebilir ve ciddi vakalarda baş oluşturmaz veya tohum üretmez. Zayıf gelişmiş kahverengi taneler nedeniyle başak uzunluğu da azalabilir.
FieldClimate modeli
Pyrenophora graminea Model
Sensörlere ihtiyaç var:
- Hava sıcaklığı
- Bağıl nem
- Yaprak ıslaklığı
- Yağış
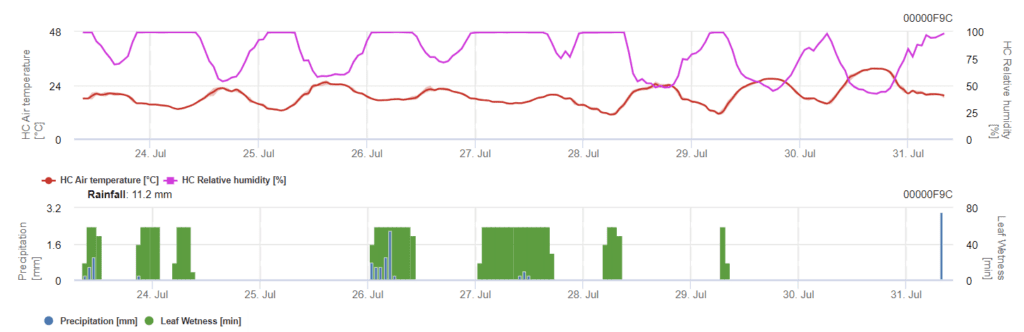
Modelde iki aşama gösterilmiştir. İlk aşama, bitkinin acil durum dönemlerindeki riskli dönemler, erken aşamalar. İkinci aşama çiçeklenme zamanı ve arpa baş gelişimi sırasındadır. Enfeksiyon 100%'ye ulaştığında, fungusun bitki dokularını enfekte etmesi ve içeride sistematik olarak büyümesi için tarlada en uygun koşullar sağlanmıştır.
Edebiyat
- Richardson, M. J. (1996). Tohum mikolojisi. Mikolojik Araştırma, 100(4), 385-392. https://ahdb.org.uk/knowledge-library/barley-leaf-stripe-life-cycle-and-disease-symptoms https://plantwiseplusknowledgebank.org/doi/full/10.1079/pwkb.species.46115
Septoria
Patojen
Buğdayda iki önemli Septoria hastalığı vardır - Septoria tritici'nin neden olduğu leke Septoria tritici ve Septoria nodorum lekesinin neden olduğu Septoria nodorum.
Septoria tritici Yaz boyunca enfekte olmuş ürün kalıntılarında hayatta kalır ve sonbaharda buğday bitkilerini enfekte etmeye başlar. Mantar serin ve nemli koşullarda gelişir. Latent faz ve nekrotik faz olmak üzere iki aşaması vardır. Latent faz sırasında, mantar yeni bitki dokusunu aşılar ve stomalardan girerek bitki dokuları içinde hücreler arası büyüdüğü kolonizasyonu takip eder. S. tritici herhangi bir fiziksel beslenme yapısına ihtiyaç duymaz, bunun yerine yapısal bütünlüğünü kaybetmiş konukçu hücrelerden besin alarak kendini besler. Bitkiler aşırı duyarlı bir tepki gösterebilir ve enfeksiyona tepki olarak etkilenen dokularda nekrotik lezyonlar gelişebilir.
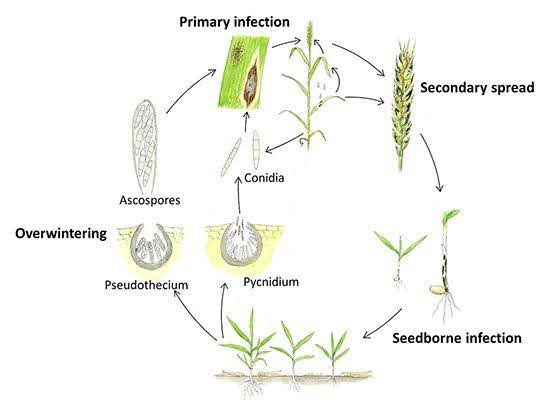
Septoria nodorum Yaz boyunca ürün kalıntıları üzerinde dormant misel, piknidya ve psödotesya olarak hayatta kalır. Enfeksiyon tipik olarak sonbaharda piknidyalardan piknidiosporların ve psödotesyalardan askosporların rüzgar ve yağmurla dağılarak birincil enfeksiyonu başlatmasıyla başlar. Bu sporlar yaprak kütikulasına nüfuz eder ve enfeksiyonun ardından piknidya oluşumu gerçekleşir. İkincil enfeksiyon, piknidiosporların üretilmesi ve alt yapraklardan üst yapraklara ve glumeslere dağılmasıyla oluşur. Patojen ayrıca hastalık gelişimine katkıda bulunan toksinler de üretir.
Semptomlar
Septoria tritici lekesi
Sonbaharda, Septoria tritici Semptomlar başlangıçta yapraklarda küçük sarı lekeler olarak ortaya çıkar ve mantar meyve gövdeleri olan küçük siyah benekler içerir. Lezyonların şekli düzensizdir, eliptikten uzun ve dar olana kadar değişir, genişler ve olgunlaştıkça kahverengiden kırmızımsı kahverengiye döner. Hastalık tipik olarak alt yapraklarda başlar ve yavaş yavaş yukarı doğru hareket ederek sonunda bayrak yaprağını etkiler. Islak koşullarda, mantar buğday başaklarına yayılabilir ve glume lekesi olarak bilinen glume ve kılçıklarda kahverengi lezyonlara neden olabilir. Septoria tritici lekesi diğer buğday hastalıklarıyla karıştırılabilir. Bununla birlikte, siyah mantar cisimciklerinin varlığı, Septoria tritici lekesinin temel bir özelliğidir. S. tritici. Septoria nodorum da ıslak koşullarda kahverengi meyve gövdeleri üretebilmesine rağmen, renk ve boyut bakımından farklılık gösterirler. Septoria tritici meyve gövdeleri daha büyüktür.
Septoria nodorum lekesi
Septoria nodorum Semptomlar ilk olarak üst yapraklarda görülür. Başlangıçta yapraklarda sarı haleli koyu kahverengi lekeler görülür. Yaprakların uç yanıkları bir başka başlangıç göstergesidir. Lezyonlar genişler ve olgunlaştıkça koyu kahverengi bir merkez ile nekrotik hale gelir. Lezyonların içinde meyve gövdeleri olan küçük koyu kahverengi yapılar görülebilir. Meyve gövdelerinden salınan konidiler beyaz ila pembe kütleler halinde görünür. Ciddi şekilde enfekte olmuş yapraklar tamamen lezyonlarla kaplanabilir ve sonunda yaprak dokusunun ölümüyle sonuçlanabilir. Fungus ayrıca glumes ve kılçıkları da etkileyebilir: benzer kahverengi lezyonlar ortaya çıkar ve hastalık aşağı doğru ilerler.
FieldClimate modeli
Septoria enfeksiyonları düşük sıcaklıklarda mümkünken, 7°C'nin altındaki sıcaklıklar 2 gün içinde enfeksiyona yol açmayabilir. Hastalığın optimum sıcaklığına 16 ila 21°C'lik bir alanda ulaşılır. Enfeksiyonlar, 14 saat veya daha uzun süreli yüksek bağıl nem veya yaprak ıslaklığı döneminde mümkündür.
Septoria tritici Modeli
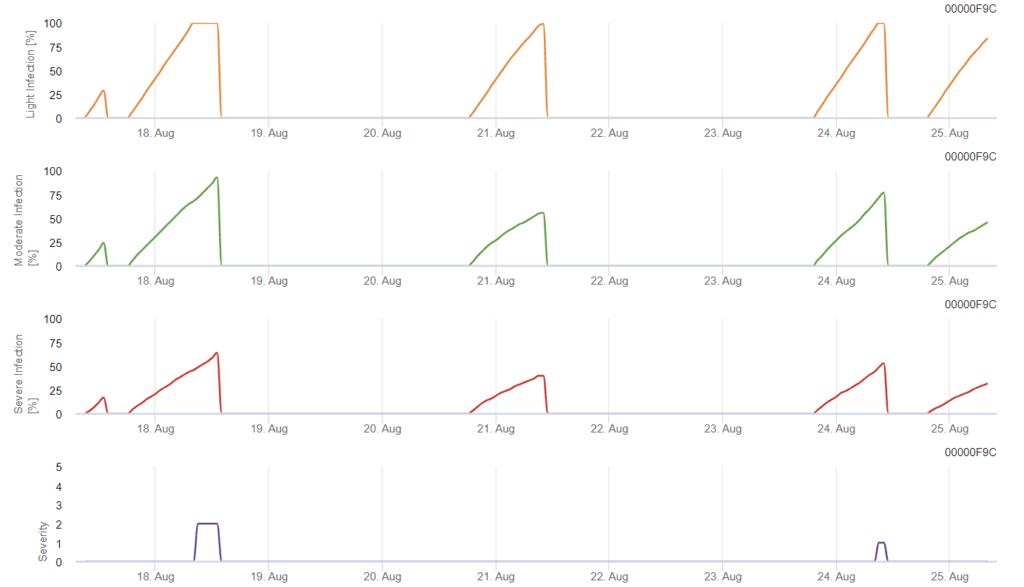
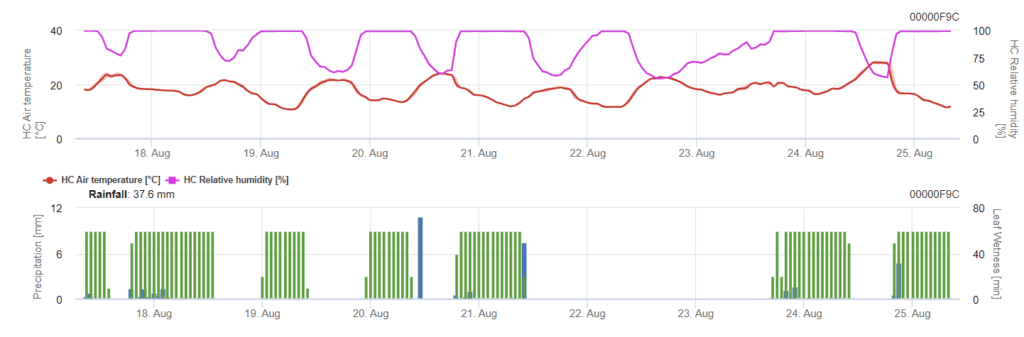
Enfeksiyon 0,5 mm'lik yağmurdan sonra başlar. Septoria enfeksiyonları için en uygun sıcaklıklar yaklaşık 16°C ila 21°C ve 14 saat boyunca yaprak ıslaklığı veya yüksek bağıl nemdir. Septoria tritici üç şiddet sınıfında hesaplanır. Ayrıca, buğdayın 10 ila 32 BBCH aşamaları arasındaki enfeksiyon baskısının değerlendirilmesini destekleyen şiddet seviyelerini belirliyoruz.
- BBCH aşama 10: Yaprak gelişimi; koleoptil boyunca ilk yaprak
- BBCH evre 32: Gövde uzaması; 2. düğüm 1. düğümden en az 2 cm yukarıda
- BBCH aşama 51: Çiçeklenme başlangıcı ve başaklanma; çiçeklenme ucu kından çıkmış ve ilk başakçık henüz görünür haldeyken başaklanma başlangıcı.
Piknidya oluşumu için bir model kullanmamaya karar verdik. Piknidya oluşumu için gereken koşulun, bağıl nemin 85%'den yüksek olduğu bir dönem olduğu varsayılmıştır. Piknidinin yaşam süresi 24 saattir. Mantarın enfekte olma şansına sahip olduğu tüm iklimlerde, neredeyse her gün güneş doğarken bu koşulu sağlayan iki saat bulacağız.
Enfeksiyon şiddeti değerlendirmesi
Değerlendirmek için Septoria tritici Enfeksiyon baskısı 10 ila 32. aşamalar arasında ve 32 ila 51. aşamalar arasında, enfeksiyonların şiddetini iklim koşullarına göre değerlendirmeliyiz. Enfeksiyon şiddeti 1 ila 5 arasında değerlendirilir:
- 1: 5 mm'den az yağmur ile zayıf enfeksiyon
- 2: 5 mm'den fazla yağmur ile zayıf enfeksiyon
- 3: 5 mm'den az yağmur ile orta derecede enfeksiyon
- 4: 5 mm'den fazla yağmurda orta derecede enfeksiyon/ 5 mm'den az yağmurda şiddetli enfeksiyon
- 5: 5 mm'den fazla yağmurla birlikte şiddetli enfeksiyon
Hastalık basıncı değerlendirmesi
Tarladaki hastalık baskısı için üç faktör vardır - iklim, tarla geçmişi ve yetiştirilen çeşidin duyarlılığı. Eğer 10. aşamadan 32. aşamaya kadar hastalık şiddeti değerlerini 4 değerinde toplayabilirsek, iklim tarafından zayıf bir hastalık baskısı bekleyebiliriz. Bu değer 6'ya ulaşırsa, orta derecede bir hastalık baskısı ve 10'a ulaşırsa, iklimden daha yüksek bir hastalık baskısı bekleyebiliriz.
Çeşidin duyarlılığını ve tarla geçmişini bilmek, bizi zayıf veya orta dereceli bir hastalık baskısı durumunda ilaçlama yapıp yapmamaya yönlendirecektir. Birikmiş değerin 10 olması, her halükarda 32. aşamada bir ilaçlamaya yol açabilir.
Daha sonraki bir aşamada ilaçlama kararı ilkbahar iklimine bağlıdır. Şiddet değerlerini 10. aşamadan 6 değerine kadar biriktirebilirsek, zayıf bir hastalık baskısı bekleyebiliriz. Bu değer 10'a ulaşırsa, orta derecede bir hastalık baskısı bekleyebiliriz ve bu değer 15'e ulaşırsa, iklim durumundan yüksek bir hastalık baskısı bekleyebiliriz.
FieldClimate'de Septoria tritici şiddeti ile birlikte üç farklı enfeksiyon şiddeti gösterilmektedir. Yağış ve uzun yaprak ıslaklık dönemleri nedeniyle, S. tritici tarafından şiddetli bir enfeksiyon için koşullar yerine getirilmiştir. Şiddet seviyeleri en yüksek değer olan 5'e ulaşır, bu da enfeksiyon için yüksek bir riskin mevcut olduğu anlamına gelir.
Septoria nodorum Modeli
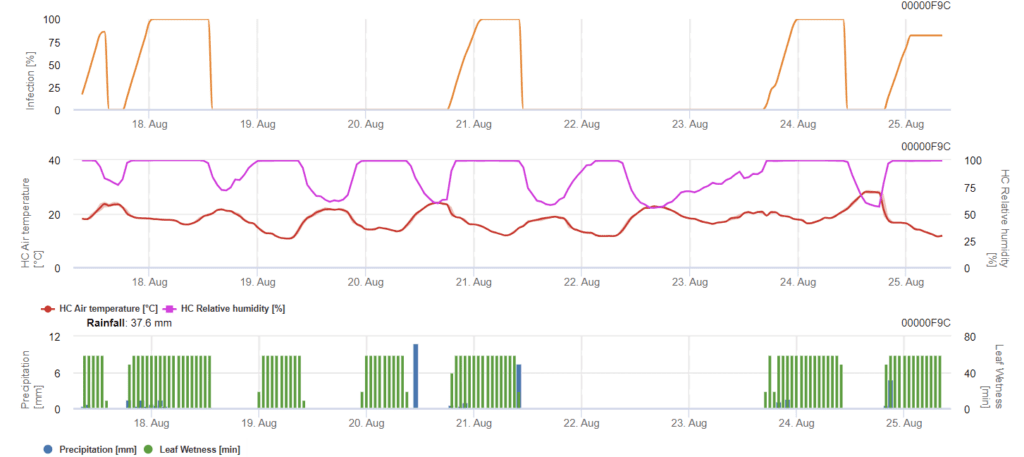
Septoria nodorum'nin enfeksiyon biyolojisi bir dereceye kadar Septoria tritici ancak aradaki fark ayrı bir model için yeterince büyük değildir. Bu nedenle, Septoria hastalığının tüm kompleksi için tritici modelinin kullanılmasını öneriyoruz. Yüksek basınçlı bölgelerde S. nodorumşiddet değeri 2 olan zayıf olarak sınıflandırılan enfeksiyonlar diğer alanlara göre daha ciddi bir şekilde ele alınmalıdır.
Bu Septoria nodorum modeli hastalık riskini hesaplar. Risk 80%'ye ulaşırsa bitki koruma önlemleri düşünülmelidir. Risk 100% olduğunda ve enfeksiyon zaten belirlendiğinde, sistemik bitki koruma önlemleri (küratif uygulamalar) alınmalıdır.
Edebiyat
- Brennan, C. J., Benbow, H. R., Mullins, E., & Doohan, F. M. (2019). Buğdayda septoria tritici leke hastalığının erken evrelerinde bilinen bilinmeyenlerin gözden geçirilmesi. Bitki Patolojisi, 68(8), 1427-1438.
- De Wolf, E. D. (2008). Septoria tritici lekesi. Mehra, L. K., Adhikari, U., Ojiambo, P. S., & Cowger, C. (2019). Buğdayda Septoria nodorum lekesi. Bitki Sağlığı Eğitmeni.
- Solomon, P. S., Lowe, R. G., TAN, K. C., Waters, O. D., & Oliver, R. P. (2006). Stagonospora nodorum: buğdayda stagonospora nodorum lekesinin nedeni. Moleküler bitki patolojisi, 7(3), 147-156.
Yaprak lekesi
Patojen
Yaprak lekesi şunlardan kaynaklanır Rynchosporium secalis.
Birincil enfeksiyon, bitki döküntüleri üzerindeki askosporlar veya konidiler tarafından meydana gelir. Bu sporlar rüzgar ve yağmurla dağılır, çimlenir ve bir enfeksiyondan sonra epidermal ve mezofil hücreleri çöktükçe semptomlar görünür hale gelir. İkincil enfeksiyon, enfekte olmuş yapraklardaki konidilerden kaynaklanır. Nemli koşullarda, konidiler yaprak yüzeyinde çimlenir ve doğrudan epidermal hücrelerin üzerindeki kütikulaya nüfuz eden hifler üretir. Sonraki fungal büyüme epidermisin subkütiküler bölgesiyle sınırlıdır.
Semptomlar
R. secalis yaprakların herhangi bir bölümünü enfekte edebilir. Düzensiz şekilli lekeler temel karakteristiktir ve enfeksiyon alttan üst yapraklara doğru başlar. Lekeler başlangıçta suyla ıslanmış alanlar olarak görünür. Hastalık ilerledikçe, spor oluşumu nedeniyle merkezde grimsi bir renk alırlar ve kenarları kahverengi olur. Nekroz ve kloroz bunu takip edebilir. Lekeler birleşerek tüm yaprakları tahrip eder.
FieldClimate modeli
Yaprak Lekesi Rynchosporium Modeli
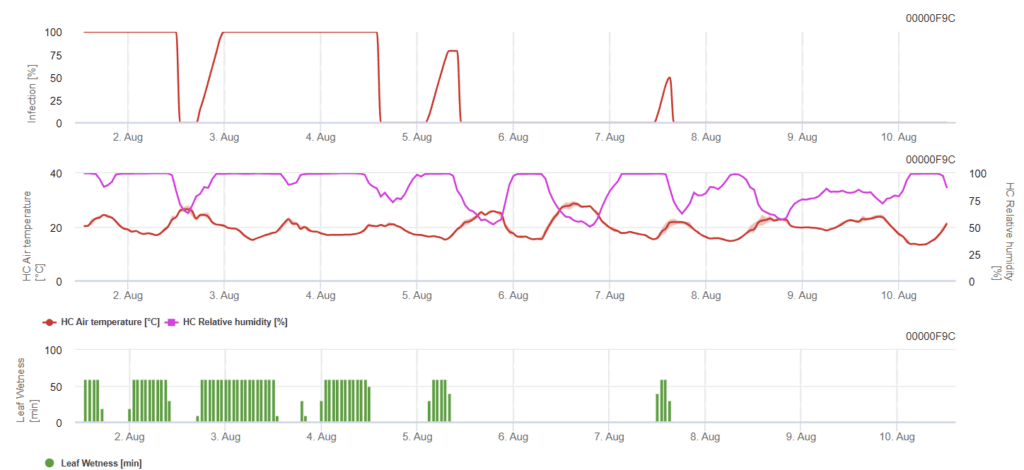
Sensörlere ihtiyaç var:
- Hava sıcaklığı
- Bağıl nem
- Yaprak ıslaklığı
Enfeksiyonun oluşması için sıcaklığa bağlı olarak (optimum 20'C) en az 7 ila 15 saatlik kurşun ıslaklığı gereklidir. Grafik 100%'ye ulaştığında, sahada optimum koşullar belirlenmiş demektir.
Edebiyat
- Brooks, F. T. (1928). Rhynchosporium secalis (Oud.) Davis, arpa ve çavdar yaprak lekesi üzerine gözlemler. New Phytologist, 27(4), 215-219.
- Fowler, A. M., & Owen, H. (1971). Arpa yaprak lekesi (Rhynchosporium secalis) üzerine çalışmalar. İngiliz Mikoloji Derneği İşlemleri, 56(1), 137-152.
- Zhan, J., Fitt, B. D., Pinnschmidt, H. O., Oxley, S. J. P., & Newton, A. C. (2008). Arpadaki Rhynchosporium secalis popülasyonlarının direnci, epidemiyolojisi ve sürdürülebilir yönetimi. Bitki patolojisi, 57(1), 1-14.
Ramularia yaprak lekesi
Patojen
Ramularia collo-cygniArpadaki Ramularia yaprak lekesinin etkeni olan fungus, öncelikle çimlenme ve erken gelişim için neme ihtiyaç duyan konidiler yoluyla eşeysiz üreme yoluyla yayılır. Yaprak yüzeyinde çimlendikten sonra, fungus stomalardan yaprağa girer ve dokuyu hücreler arası kolonize eder. Enfekte arpa bitkileri başlangıçta hiçbir belirti göstermeyebilir, ancak hasar tipik olarak çiçeklenmeden sonra ortaya çıkar.
Yaşam döngüsü R. collo-cygni tam olarak anlaşılamamıştır, ancak enfekte tohumlar yoluyla dikey bulaşmayı içerir ve patojenin büyüme mevsimleri arasında hayatta kalmasına izin verir. Hava yoluyla taşınan konidiler de ikincil yayılmaya katkıda bulunarak uygun koşullar altında yeni enfeksiyonlar başlatır. Tohumlar birincil kışlama mekanizması olsa da, alternatif konakçıların rolü ve ikincil bir fungal yapı olan Asteromella belirsizliğini korumaktadır ve halen çalışma aşamasındadır.
Semptomlar

Belirtiler genel olarak çiçeklenmeden sonra yaprakların her iki tarafında görülür ancak üst yapraklarda daha yaygındır. İlk belirtiler yaprak damarlarında klorotik bir haleyle çevrili sarı-kahverengi lekeler şeklinde görülür. Yaprak lekeleri ortaya çıktıktan sonra, yaprak klorotik ve nekrotik hale gelir, tipik olarak yaprak ucu ve kenarlarından başlar. Komşu lekeler birleşerek daha büyük karanlık alanlar oluşturabilir. Küçük punktiform lekeler de görülebilir. Ramularia yaprak lekesi semptomları diğer hastalıklarla karıştırılabilse de, temel özellik yaprak lekelerinin yaprak damarlarıyla sınırlandırılmış olmasıdır.
Ramularia yaprak lekelerini ayırt etmek için 5R olarak adlandırılan bir yöntem vardır:
- Sarı bir kloroz kenarı ile halkalı
- Dikdörtgen şekil
- Yaprak damarları tarafından sınırlandırılmış
- Kırmızımsı kahverengi renk
- Tam yaprağın içinden
FieldClimate Model
Ramularia Modeli
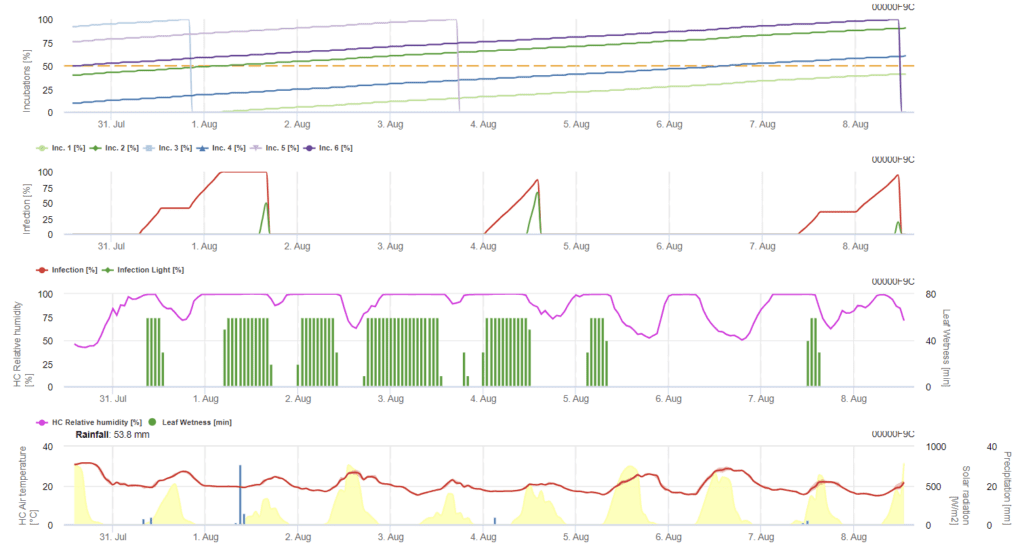
Arpadaki Ramularia enfeksiyonu çoğunlukla nemli koşullardan kaynaklanır. Bu nedenle, hesaplamaya bir yağmur olayı ve ardından 85%'den daha yüksek yaprak ıslaklığı veya bağıl nem ile başlıyoruz.
Tanımlanan iki enfeksiyon yolu vardır:
- Enfeksiyon: Nemli koşulların sadece bir enfeksiyon olayını teşvik ettiği durumlarda
- Enfeksiyon: Bir enfeksiyon olayını bitirmek için küresel radyasyon gerektiğinde bir kez
Daha sonra, 100% enfeksiyonuna ulaşıldığında, model inkübasyon süresini belirlemeye başlar. İnkübasyon 50%'ye ulaştığında, yeni inokulum için alanın kontrol edilmesi önerilir ve 100%'ye ulaştığında yapraklarda nekrotik lezyonlar öngörülür.
Edebiyat
- Havis, N. D., Brown, J. K., Clemente, G., Frei, P., Jedryczka, M., Kaczmarek, J., ... & Hess, M. (2015). Ramularia collo-cygni-arpa bitkilerinde yeni ortaya çıkan bir patojen. Phytopathology, 105(7), 895-904.
- Huss, H. (2002, Nisan). Ramularia collo-cygni'nin biyolojisi. In Proc. İkinci Uluslararası Arpa Yaprak Yanıklığı Çalıştayı. Halep, Suriye (s. 321-328).
- Walters, D. R., Havis, N. D., & Oxley, S. J. (2008). Ramularia collo-cygni: yeni ortaya çıkan bir arpa patojeninin biyolojisi. FEMS Mikrobiyoloji Mektupları, 279(1), 1-7. https://grdc.com.au/__data/assets/pdf_file/0025/443509/GRDC_FS2103_Ramularia_03.pdf
Rhizoctonia solani
Patojen
Buğdayda Rhizoctonia kök çürüklüğüne şunlar neden olur Rhizoctonia solani. Patojen toprakta sklerotia olarak uzun yıllar hayatta kalabilir. Bazı durumlarda, bitki kalıntıları üzerinde misel olarak da hayatta kalır. Sıcaklık yükseldiğinde, sklerotia aktif hale gelir ve bir hif kütlesi oluşturarak köklere tutunarak enfeksiyonu mümkün kılar. Miselyum "enfeksiyon yastıkları" üretir ve mantar kök dokusunu istila edip kolonize olur. Kök enfeksiyonu fideleri zayıflatarak zayıf büyümeye neden olur ve su ve besin maddelerini toprak üstü bitki dokularına taşıma kapasitesini azaltarak sonunda bitki ölümüne yol açar.
Semptomlar
Erken dönemde, birkaç santimetreden birkaç metre çapa kadar değişen boyutlarda çıplak lekeler ortaya çıkar. Bu çıplak lekeler genellikle sararma, solma ve hatta mor renklenme gösterebilen bodur bitkilerle ilişkilidir. Enfekte bitkiler ciddi şekilde bodurlaşabilir ve kuraklık stresi veya besin eksikliği belirtileri gösterebilir, bu da bazı durumlarda erken ölüme yol açabilir.
Toprak çizgisinin altındaki gövde ve köklerde kırmızımsı kahverengi lezyonlar gelişir ve hastalık ilerledikçe bu lezyonlar çöker. Kök çürüklüğü nodülasyonu azaltabilir ve kök korteksinin kolayca kırılabilir olmasına neden olarak kahverengi mızrak uçlarına yol açabilir.
FieldClimate modeli
Rhizoctonia solani Risk Modeli
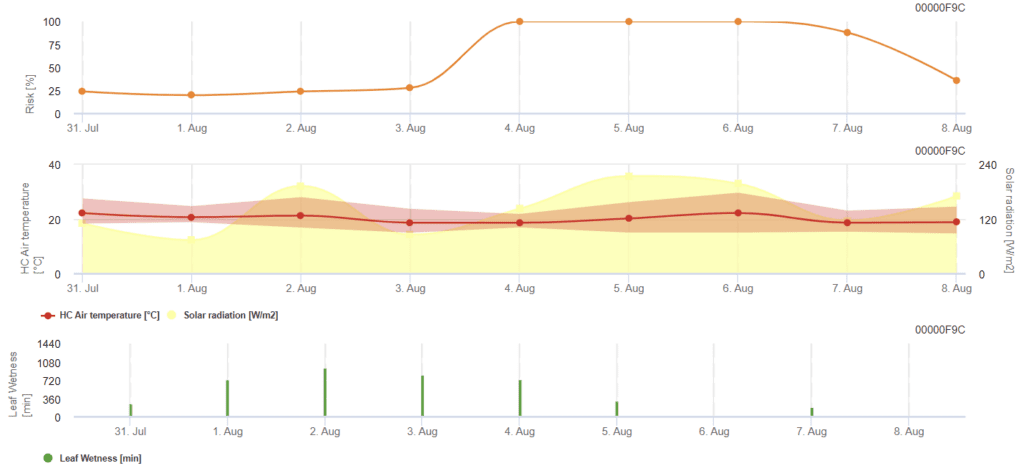
Sensörlere ihtiyaç var:
- Hava sıcaklığı
- Güneş radyasyonu
- Yaprak ıslaklığı
Model, riskli dönemleri hesaplar Rhizoctonia solani Son 120 saatin koşullarını kontrol ederek. Hastalık için elverişli koşulları gösteren 0 ila 100 arasında bir risk değeri ile sonuçlanır.
Risk düşük olduğunda spreylemeye gerek yoktur. Orta riskli dönemlerde sprey aralığı uzatılabilir ve yüksek riskli dönemlerde azaltılması gerekebilir veya daha etkili bileşik kullanımı önerilebilir.
Ardışık yaprak ıslaklığı durumunda, her dakika için sıcaklığa bağlı değerleri biriktirir:
- 12 °C ila 15 °C: dakikada 1 birikme
- 16 °C ila 17 °C: dakikada 2 birikme
- 18°C ve üzeri: dakikada 4 birikim
Yaprak ıslaklık dönemlerinin sonunda biriken değerleri değerlendirir:
- Değerler > 4096: Risk 64 puan artar ve değerden 4096 çıkarılır
- Kalıntı değerleri > 2048: Risk 16 puan artar ve değerden 2048 çıkarılır
- Kalıntı değerleri >1024: Risk 4 artar ve değerden 1024 çıkarılır
Küresel radyasyon 800 W/m²'den daha yüksekse, dakika cinsinden zaman biriktirir ve radyasyon düştüğünde değerleri değerlendirir:
- Değer > 512: Risk - 32 puan, değer - 512
- Değer > 256: Risk - 8 puan, değer - 256
- Değer > 128: Risk - 2 puan, değer - 128
Edebiyat
- https://cropprotectionnetwork.org/encyclopedia/rhizoctonia-root-rot-of-wheat#:~:text=It%20is%20caused%20by%20Rhizoctonia,result%20in%20premature%20plant%20death.
- https://ahdb.org.uk/knowledge-library/rhizoctonia-stunt-symptoms-and-risk-in-cereals
- https://cropwatch.unl.edu/rhizoctonia-root-rot#:~:text=Disease%20Symptoms&text=These%20reddish%20brown%20lesions%20may,uneven%20because%20of%20stunted%20plants.
- https://extensionaus.com.au/FieldCropDiseasesVic/docs/identification-management-of-field-crop-diseases-in-victoria/soil-borne-diseases/rhizoctonia-root-rot/
- https://www.florimond-desprez.com/es/wp-content/uploads/sites/6/2015/11/rhizoctonia_eng.pdf
Toz halinde küf
Patojen
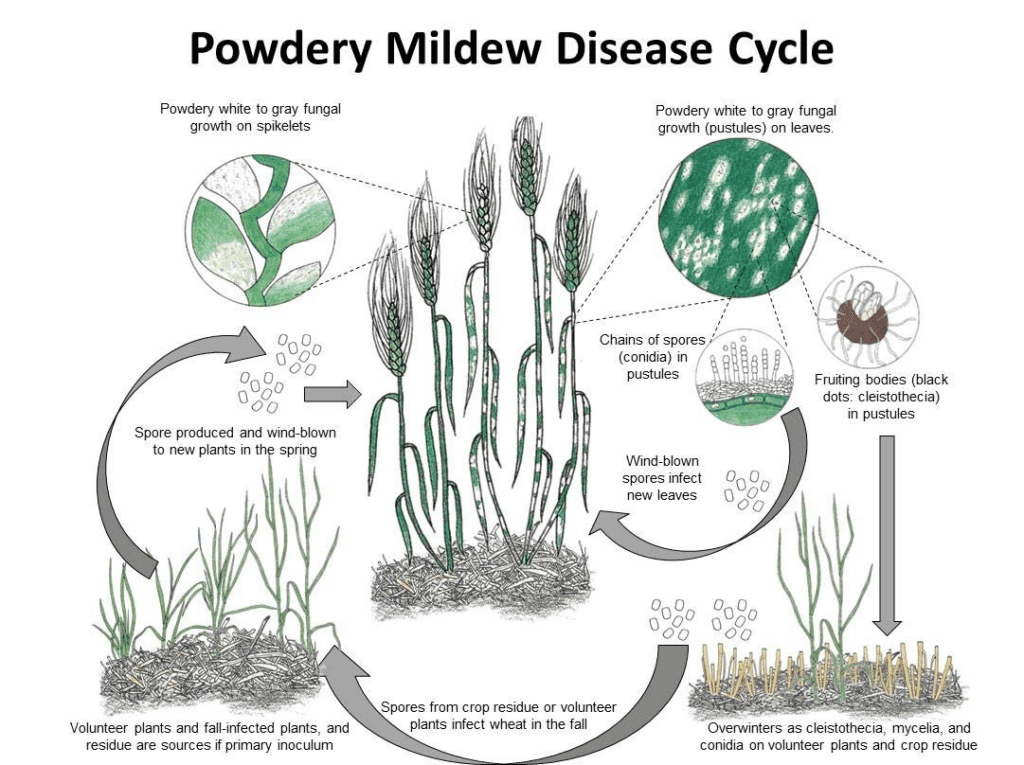
Blumeria graminis buğday ve arpada külleme hastalığının patojenidir. Kışı misel veya kleistotesyum olarak geçirebilir. İlkbaharda sporlar çimlenir ve bitki yüzeylerinde serbest suya ihtiyaç duymadan serin ve nemli koşullar altında konukçu bitkileri enfekte eder.
Mantar hem eşeysiz hem de eşeyli olarak çoğalır.
Eşeysiz döngüde patojen, hastalığın yayılmasında kilit rol oynayan hızlı enfeksiyon ve konidya (eşeysiz sporlar) üretim döngülerinden geçer. Uygun koşullar altında miselyumda her 7 ila 10 günde bir konidya üretilir. Bu konidiler rüzgarla dağıldıktan sonra yeni bir konukçuya konar, çimlenir ve bitkiden besin almak için appressoria ve haustoria oluşturur. Blumeria graminis konidileri düşük nem ve çeşitli sıcaklıklarda bile çimlenebilir.
Cinsel döngüde mantar, olumsuz koşullarda iyi bir şekilde hayatta kalabilen dayanıklı yapılar olan cleistothecia üretir. Cleistothecia askosporlar (eşeyli sporlar) içerir ve bu sporlar serbest kaldığında yeni enfeksiyonlar başlar.
Semptomlar

Buğday ve arpadaki külleme, başak sayısını azaltarak ve tane boyutunu ve ağırlığını düşürerek tane verimini etkiler. Enfeksiyon ne kadar erken ortaya çıkarsa, zarar o kadar büyük olacaktır.
Arpa, küllemeye karşı yaşa bağlı direnç gösterir. Arpa olgunlaştıkça, tipik miselyum lekeleri yerine, yapraklarda keskin bir şekilde tanımlanmış, siyah-kahverengi lekeler ("katran lekeleri") görülebilir.
Buğday, özellikle bayrak yapraklar ve kabuklar etkilendiğinde, kardeşlenme ve süt olgunluğu dönemi arasında küllemeye karşı özellikle hassastır. Bununla birlikte, arpaya kıyasla buğday erken enfeksiyonları daha iyi tolere edebilir.
Beyaz-grimsi külleme yapraklarda, gövdelerde ve başlarda gelişir. Mantar büyümesi en çok üst yaprak yüzeyinde belirgindir, ancak alt tarafta da gelişebilir. Başlangıçta püstüller beyaz görünür ancak olgunlaştıkça yavaş yavaş griden kahverengiye döner ve birleşerek genellikle klorozla çevrili daha büyük kütleler oluşturabilirler. Enfekte yaprakların karşı tarafında dokular sararır, daha sonra ten rengi veya kahverengiye döner. Cleistothecia eski gri koloniler içinde küçük, yuvarlak, siyah noktalar olarak da görülebilir. Ağır vakalarda yapraklar ölebilir.
FieldClimate modeli
Buğday Küllemesi Modeli
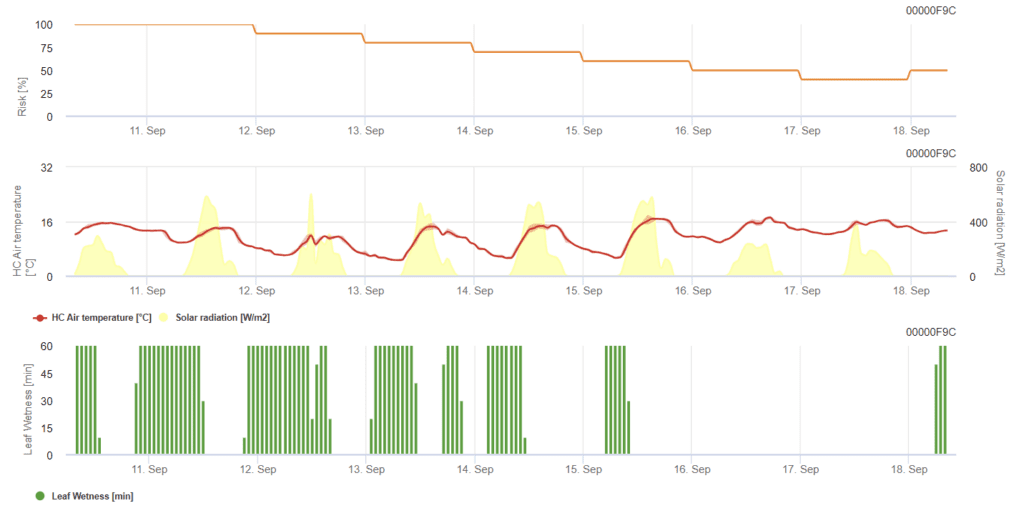
Sensörlere ihtiyaç var:
- Hava sıcaklığı
- Yaprak ıslaklığı
- Güneş radyasyonu
Model, 0 (enfeksiyon yok) ile 100% (tam enfeksiyon) arasında değişen bir ölçekte külleme riskini belirler. Arpa için 21 ila 39, buğday ve yulaf için 21 ila 75 BBCH evresi boyunca geçerlidir.
BBCH aşaması, bitkilerin gelişimini tanımlamak için kullanılan bir büyüme ölçeğidir. İki basamaktan oluşan ölçek 00 ile 99 arasında değişir - 00 tohum işlemini, 99 ise hasat sonrası işlemin gerçekleştiği zamanı ifade eder. İlk rakam gelişimin spesifik aşamasını gösterir; 0 çimlenme, 1 yaprak gelişimi, 2 toprak işleme, 3 gövde uzaması, 4 önyükleme, 5 çiçeklenme ve başaklanma, 6 çiçeklenme ve antez, 7 meyve gelişimi, 8 olgunlaşma ve 9 yaşlanmadır.
- BBCH 21: Kardeşlenme - Kardeşlenme başlangıcı; ilk kardeşlenme tespit edilebilir.
- BBCH 39: Gövde uzaması - bayrak yaprağı aşaması; bayrak yaprağı tamamen açılmış ve ligül sadece görünür.
- BBCH 75: Meyve gelişimi - orta sütlü; tane içeriği sütlü ve taneler son boyuta ulaşır ancak hala yeşildir.
Günün çoğu saatinde 12°C ile 21°C arasındaki sıcaklıklarda ve düşük küresel radyasyonda risk artmaktadır. Buna karşılık yaprak ıslaklığı, yüksek küresel radyasyon ve 32°C'nin üzerindeki yüksek sıcaklıklar riski azaltır.
Edebiyat
- Both, M., & Spanu, P. D. (2004). Blumeria graminis f. sp. hordei, arpanın zorunlu bir patojeni. Yıllık Bitki İncelemeleri, 11, 202-218.
- Cunfer, B. M. (2002). Külleme. Ekmeklik Buğday: Islahı ve Üretimi, 30, 317-330.
- Der Gräser, E. M. Krankheiten und Schädlinge des Getreides. Lancashire, P. D., Bleiholder, H., Boom, T. V. D., Langelüddeke, P., Stauss, R., Weber, E., & Witzenberger, A. (1991). Bitkilerin ve yabani otların büyüme aşamaları için tek tip bir ondalık kod. Annals of applied Biology, 119(3), 561-601. https://ohioline.osu.edu/factsheet/plpath-cer-11
Kahverengi pas
Patojen
Üç önemli pas ve patojen vardır:
- Yaprak / Kahverengi pas: Puccinia triticina
- Kök/ Siyah pas: Puccinia graminis
- Şerit/ Sarı pas: Puccinia striiformis
Kahverengi pas en yaygın buğday pası hastalığıdır. Kara pas, bol miktarda parlak siyah teliospor gelişimi nedeniyle yaz pası olarak da bilinir. En yıkıcı pas hastalığıdır ve uygun koşullar altında bir ay içinde kayıpların yüzde 50'sine neden olur. Sarı pas, daha serin iklimlerde, genellikle yüksek rakımlarda ve kuzey enlemlerinde görülen bir buğday hastalığıdır. Karakteristik özelliği sarı renkli urediniosporlarıdır. Şiddetli vakalarda kara pas kadar önemli hasara da neden olabilir.
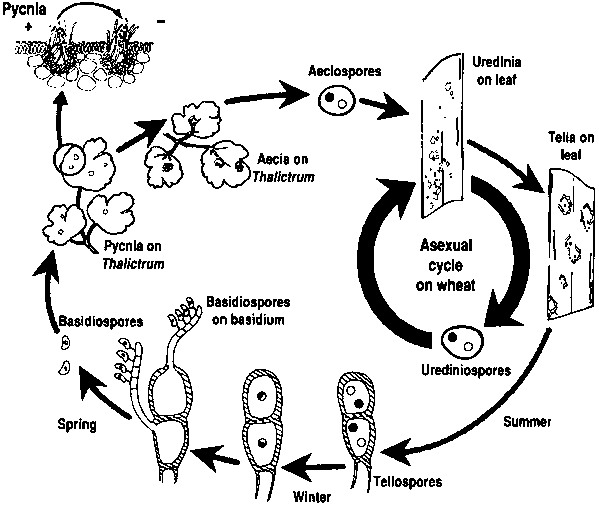
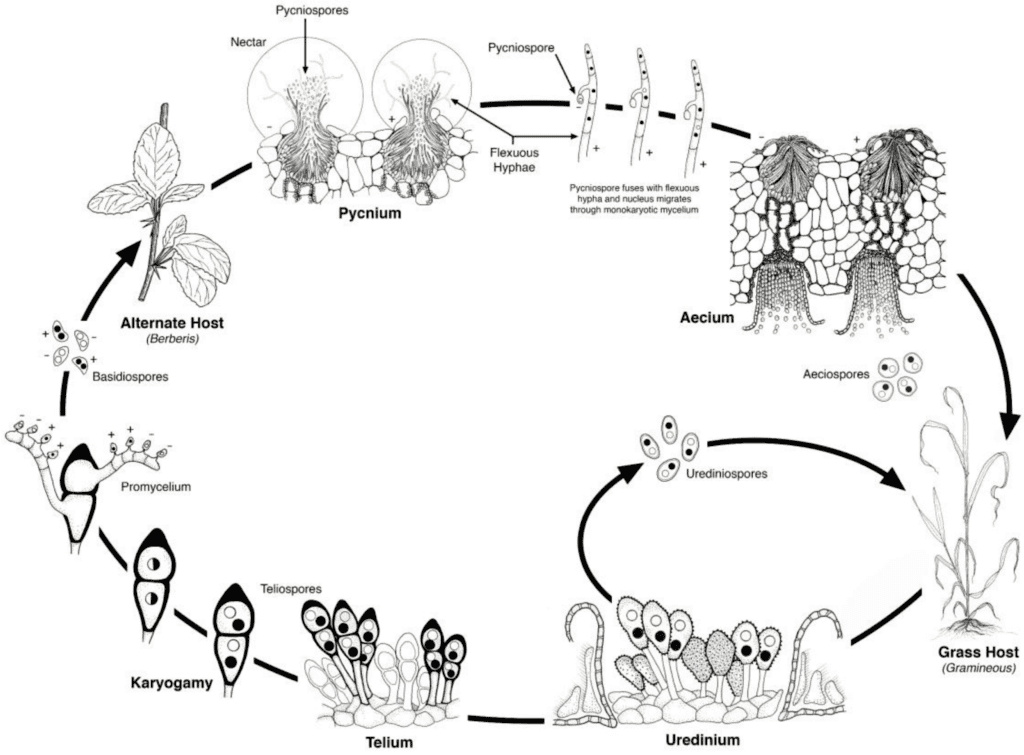
Buğday pası patojenleri hem eşeysiz hem de eşeyli üreme döngülerinden geçer ve bir ekonomik konukçu ve bir de alternatif konukçu olmak üzere iki konukçu bitkiye ihtiyaç duyar. Ekonomik konukçu buğdaydır ve alternatif konukçu tipik olarak mantarların eşeyli aşamadan geçmesini sağlayan bir yabani ot veya yerli bitkidir. Puccinia striiformis uredinial ve telial evrelerden oluşan herhangi bir alternatif konağa sahip olduğu bilinmemektedir.
Eşeysiz döngüde, urediniosporlar konakçı bitki üzerinde üretilir ve bitkiyi tekrar tekrar enfekte etmeye devam ederek uygun koşullar altında hızlı ve yaygın enfeksiyona yol açabilir.
Patojenin eşeyli döngüsü, konukçu bitki üzerindeki üredinial enfeksiyonlarda oluşan teliosporların çimlenmesi ve bazidiospor üretmek için mayoz bölünme geçirmesiyle başlar. Bu basidiosporlar alternatif bir konukçuya dağılır ve burada enfeksiyonu başlatarak pycniosporlar ve alıcı hifler içeren pycnia oluşumuyla sonuçlanır. Döllenme, bir çiftleşme türünden gelen pikniyosporların nektar yoluyla diğerine aktarılmasıyla gerçekleşir. Döllenmeyi takiben, alternatif konağın yapraklarının alt tarafında aecial kupalar gelişir ve bunlar aeciosporları serbest bırakır. Bu aeciosporlar dağılır ve yeni konukçuları enfekte eder, üredinial enfeksiyon bunu takip ederek patojenin yaşam döngüsünü tamamlar.
Semptomlar

A) Puccinia graminis
B) Puccinia striiformis
C) Puccinia triticina
Puccinia triticina
P. triticina Öncelikle yaprak kanatlarını enfekte eder, ancak bazen yaprak kılıflarını, glumları ve kılçıkları da etkileyebilir ve üst yaprak yüzeyinde küçük sarı lekeler oluşturur. Bu lekeler hastalık ilerledikçe sarı bir haleyle çevrili turuncu renkli püstüllere dönüşür. Püstüller yapraklarda görülebilen turuncu veya siyah sporlar üretir. Kara pasın aksine daha az teliospor üretir. Bazılarında klorotik veya nekrotik alanlarla çevrili aşırı duyarlı benekler veya ürinia görülebilir.
Puccinia graminis
P. graminis Esas olarak gövdeleri hedef alır, ancak yaprakları, kılıfları, glumları, kılçıkları ve hatta tohumları da enfekte edebilir. Başlangıçta kırmızımsı kahverengi lezyonlar ortaya çıkar ve hastalık ilerledikçe püstüller içinde siyah teliosporlar oluşur. Kırmızı tuğlalı urediniospor yığınları ilk olarak saplarda ve yaprak kılıflarında gelişir ve küçük klorotik benekler ortaya çıkar, bunlar doğrusal veya elmas şekilli püstüllere dönüşür ve boyutları genişleyebilir. Olgunlaştıkça, urediniospor üretimi durur ve siyah teliospor tabakası üretilir, bu da sezonun sonlarında gövdelerin kararmış görünmesine neden olur. Şiddetli vakalarda enfeksiyon bitki gövdelerini zayıflatarak yatmaya yol açar.
Puccinia striiformis
Karakteristik özelliği P. striiformis düz kenarlı sarı püstüllerin varlığıdır. TJey, genellikle kloroz ve nekrozun eşlik ettiği, çeşitli uzunluklarda dar, uzun şeritler halinde görülür. Hastalık olgunlaştıkça, püstüllerin içinde sarı-turuncu sporlar gelişir ve çevre dokular kahverengiye dönerek kurur ve kavrulmuş bir görünüm oluşturur.
FieldClimate modeli
Puccinia Pas Modeli
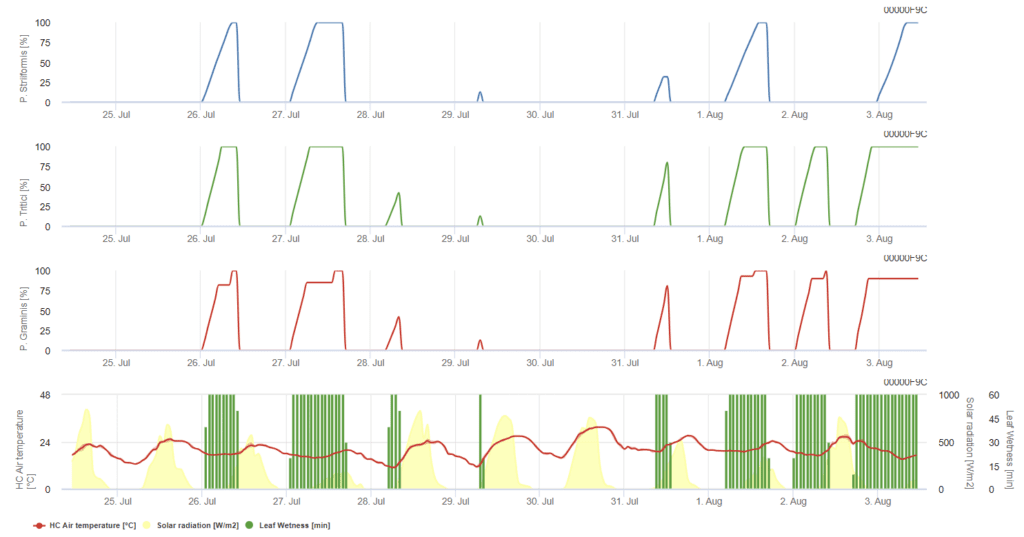
P. triticina, P. graminis, P. striiformis her biri üç farklı renkli grafikte sunulmuştur.
Puccinia triticna Enfeksiyon Modeli
Model, enfeksiyonun 5°C ila 30°C hava sıcaklığı aralığında 90°C yaprak ıslaklığı birikmiş saatlik sıcaklığa ihtiyaç duyduğunu varsayar. Koşullar şuna benzer P. graminisancak 5°C'lik daha düşük bir sıcaklık eşiği ile.
100% enfeksiyon gösterilirse, iyileştirici bir bitki koruma ölçümü düşünülmelidir. Risk 80%'de ise ve hava tahmini daha fazla yaprak ıslaklık dönemi öngörüyorsa, koruyucu yaprak uygulamaları alınabilir.
90°C için birikmiş saatlik ortalama sıcaklıklar için yaprak ıslaklığı:
- (eğer T <= 22,5°C ise ∑(Th) aksi takdirde ∑ (22,5-(Th-22,5))
- 5°C < Sıcaklık. < 30°C
Puccinia graminis Enfeksiyon Modeli
Enfeksiyonlar, optimum sıcaklık koşullarında birkaç saatlik yaprak ıslaklığından sonra gerçekleşir. Model, enfeksiyonun 10°C ila 35°C hava sıcaklığı aralığında 80°C yaprak ıslaklığı birikmiş saatlik sıcaklığa ihtiyaç duyduğunu varsayar. Bu sıcaklıktan biraz daha yüksek bir sıcaklığı tercih eder. P. triticina ve enfeksiyonu güneş ışığının takip etmesi gerekir.
100% enfeksiyonu gösterildiğinde, koşullar fungus için elverişlidir ve bu nedenle bitki koruma önlemleri dikkate alınmalıdır.
80°C için birikmiş saatlik ortalama sıcaklıklar için yaprak ıslaklığı ve ardından 30°C için birikmiş saatlik ortalama sıcaklıklar için bir ışık periyodu (150 W/m²):
- (T <= 24°C ise ∑(Th), aksi takdirde ∑(Th-24))
- 10°C < Sıcaklık. < 35°C
Puccinia striiformis Enfeksiyon Modeli
Puccinia striiformis optimum sıcaklığı 15°C'den itibaren olan serin iklimlerin buğday pasıdır. Enfeksiyonlar, optimum sıcaklık koşullarında birkaç saatlik yaprak ıslaklığından sonra gerçekleşir. Model, enfeksiyonun 5°C ila 20°C hava sıcaklığı aralığında 80°C yaprak ıslaklığının birikmiş saatlik sıcaklığına ihtiyaç duyduğunu varsayar. Işık yoğunluğunun düşük olduğu dönemlerde enfeksiyon görülmez.
Grafik 100%'ye ulaşmadan önce koruyucu uygulama yapılabilirken, ulaştıktan sonra iyileştirici koruma stratejileri (sistemik) düşünülmelidir.
80°C için birikmiş saatlik ortalama sıcaklıklar için yaprak ıslaklığı ve ışık:
- (T <= 15°C ise ∑(Th), değilse ∑(Th-15))
- 5°C < Sıcaklık. < 20°C
Edebiyat
- Bolton, M. D., Kolmer, J. A., & Garvin, D. F. (2008). Puccinia triticina'nın neden olduğu buğday yaprak pası. Moleküler bitki patolojisi, 9(5), 563-575.
- Chen, X. M. (2005). Buğdayda şerit pas [Puccinia striiformis f. sp. tritici] epidemiyolojisi ve kontrolü. Kanada Bitki Patolojisi Dergisi, 27(3), 314-337.
- Figueroa, M., Hammond-Kosack, K. E., & Solomon, P. S. (2018). Buğday hastalıkları üzerine bir inceleme - tarla perspektifi. Moleküler bitki patolojisi, 19(6), 1523-1536.
- Guide, A. Buğdayda Yaprak, Sap ve Çizgili Pas Hastalıkları. Leonard, K. J., & Szabo, L. J. (2005). Puccinia graminis'in neden olduğu küçük tahıl ve otların kök pası. Moleküler bitki patolojisi, 6(2), 99-111.
- Kolmer, J. (2013). Buğdayda yaprak pası: patojen biyolojisi, varyasyon ve konukçu direnci. Ormanlar, 4(1), 70-84.
- Singh, R. P., Huerta-Espino, J., Roelfs, A. P., & Curtis, B. C. (2002). Buğday pasları. Büyüme, 2(25), 35.
Önerilen ekipman
Bu ürünün potansiyel hastalıklarını izlemek için hangi sensör setinin gerekli olduğunu kontrol edin.
