
Weizen Krankheitsmodelle
Weizensprengung
Krankheitserreger
Pyricularia grisea, auch bekannt als Magnaporthe oryzaeist ein pilzlicher Krankheitserreger, der für die Weizenblasenbildung verantwortlich ist, eine bedeutende Krankheit im Weizenanbau. Der Erreger vermehrt sich in erster Linie ungeschlechtlich durch Konidien (ungeschlechtliche Sporen), die als primäres Inokulum für die Auslösung von Infektionen dienen. Diese Konidien werden auf Konidiophoren produziert und durch Wind, Regen und mechanische Mittel, wie z. B. landwirtschaftliche Geräte, verbreitet. Wenn sie auf einem anfälligen Weizenwirt landen, keimen die Konidien und bilden Appressorien - spezialisierte Strukturen, die das Eindringen in das Pflanzengewebe erleichtern. Dort kolonisiert der Pilz die Wirtszellen, was zur Entwicklung der Krankheit führt. Die Umweltbedingungen spielen eine entscheidende Rolle im Infektionsprozess von P. grisea. Der Pilz gedeiht in warmem, feuchtem Klima mit Temperaturen zwischen 15°C und 30°C und längeren Perioden von Blattnässe oder hoher relativer Luftfeuchtigkeit. Eine kontinuierliche Blattnässe von mindestens 14 Stunden ist notwendig, um eine Infektion auszulösen, so dass übermäßige Bewölkung, hohe Luftfeuchtigkeit, Überbewässerung und falsch getimte Bewässerung die Entwicklung der Krankheit begünstigen. Darüber hinaus können Stressfaktoren wie Trockenheit, Bodenverdichtung, niedrige Schnitthöhen und übermäßige Stickstoffdüngung den Schweregrad der Krankheit verschlimmern.
Symptome
Die ersten Symptome der Weizenbräune zeigen sich als wassergetränkte, rautenförmige Läsionen auf den Blättern, die sich im weiteren Verlauf der Krankheit grau verfärben. Diese Läsionen können sich ausdehnen und zusammenwachsen, was zu ausgedehntem Blattbefall und Nekrose führt. Befallene Ähren bleichen teilweise oder vollständig aus, oft ausgehend von einem schwärzlich-grauen Infektionspunkt an der Spindel oder an der Basis der Ähren. Bei hohem Inokulumdruck können mehrere Infektionspunkte an einer einzigen Rispe auftreten, was zu erheblichen Ertragseinbußen führt. Zusätzlich zu den Blattsymptomen, P. grisea kann andere oberirdische Teile der Weizenpflanze, einschließlich der Knoten und Hälse, infizieren, was zu einer Fäulnis der Hälse oder einer Knotenblast führt. Dies kann dazu führen, dass die befallenen Teile aufbrechen, was zu Lagerbildung und weiteren Ertragseinbußen führt. Die Fähigkeit des Erregers, verschiedene Pflanzenteile während der gesamten Vegetationsperiode zu infizieren, macht ihn besonders zerstörerisch, vor allem unter günstigen Umweltbedingungen.
Modell FieldClimate
Benötigte Sensoren:
- Lufttemperatur
- Relative Luftfeuchtigkeit
- Blattnässe
Bewölkter Himmel, feuchte Bedingungen und Nieselregen begünstigen die Entwicklung und den Schweregrad der Krankheit. In FieldClimate werden drei Schweregrade berechnet, und wenn 100% der Infektion erreicht sind, sind optimale Bedingungen für den Pilzerreger im Feld gegeben. In Abhängigkeit von der Sorte sind bei Erreichen von 100% leichter, mittlerer oder schwerer Infektion feldgeschichtliche kurative Pflanzenschutzmaßnahmen zu berücksichtigen.
Literatur
- Cruz, C. D., & Valent, B. (2017). Die Weizenblastkrankheit: Gefahr im Anmarsch. Tropische Pflanzenpathologie, 42(3), 210-222.
- Islam, M. T., Croll, D., Gladieux, P., Soanes, D. M., Persoons, A., Bhattacharjee, P., ... & Talbot, N. J. (2016). Das Auftreten der Weizenblast in Bangladesch wurde durch eine südamerikanische Linie von Magnaporthe oryzae verursacht. BMC Biologie, 14(1), 84.
Pyrenophora teres
Krankheitserreger
Pyrenophora teres (Drechslera teres) existiert in zwei Formen - P. teres f. teres und P. teres f. maculata die netzförmige Netzflecken bzw. punktförmige Netzflecken hervorrufen.
Die aus den Pseudothecien freigesetzten Ascosporen infizieren die Rückstände und lösen die Primärinfektion aus. In einigen Fällen dienen auch samenbürtige Myzelien und Konidien als Primärinokulum. Die Sporen keimen auf Blättern und durchdringen die äußere epidermale Zellwand, so dass sich der Erreger in einem großen intrazellulären Vesikel entwickeln kann. Es folgt das asexuelle Stadium, in dem Konidien gebildet werden, die die Sekundärinfektion auslösen und den Schweregrad der Krankheit erhöhen. Am Ende der Vegetationsperiode produziert der Erreger Pseudothecien, die auf infizierten Gerstenresten verbleiben und als Überwinterungsquelle dienen.
Symptome
Die Symptome treten an Blättern, Stängeln und Kernen auf, wobei sich die Krankheit von unten nach oben ausbreitet. Ältere Pflanzen werden in der Regel weniger stark geschädigt, da sie eine dickere Kutikula haben, die das Eindringen des Erregers verhindert, und eine größere Fähigkeit, antimykotische Verbindungen zu produzieren. Die Krankheitserreger produzieren Toxine, die für die Symptome verantwortlich sind und zu Nekrose und Chlorose beitragen oder den Wasserhaushalt auf zellulärer Ebene stören.
Bei der Netzfleckenkrankheit erscheinen die Symptome als schmale, dunkelbraune, längliche Läsionen. Bei hochresistenten Sorten entwickeln sich nur wenige kleine punktförmige Läsionen, ohne dass sich ein ausgeprägtes netzartiges Muster bildet. Im Gegensatz dazu können die meisten anfälligen Sorten chlorotische oder wassergetränkte Bereiche aufweisen, die die nekrotischen Läsionen umgeben.
Bei der Fleckenkrankheit bestehen die Symptome aus dunkelbraunen, kreisförmigen oder elliptischen Läsionen, die oft von einem chlorotischen oder nekrotischen Lichthof unterschiedlicher Breite umgeben sind. Bei weniger anfälligen Sorten sind die Läsionen in der Regel kleiner und können ohne einen umgebenden chlorotischen Lichthof sein.
Schwere Infektionen können zum vollständigen Absterben der Blätter führen, so dass diese trocken erscheinen. Ältere Blätter welken in der Regel zuerst, gefolgt von den jüngeren Blättern.
Modell FieldClimate
Drechslera teres Modell
Benötigte Sensoren:
- Lufttemperatur
- Relative Luftfeuchtigkeit
- Blattnässe
- Niederschlag
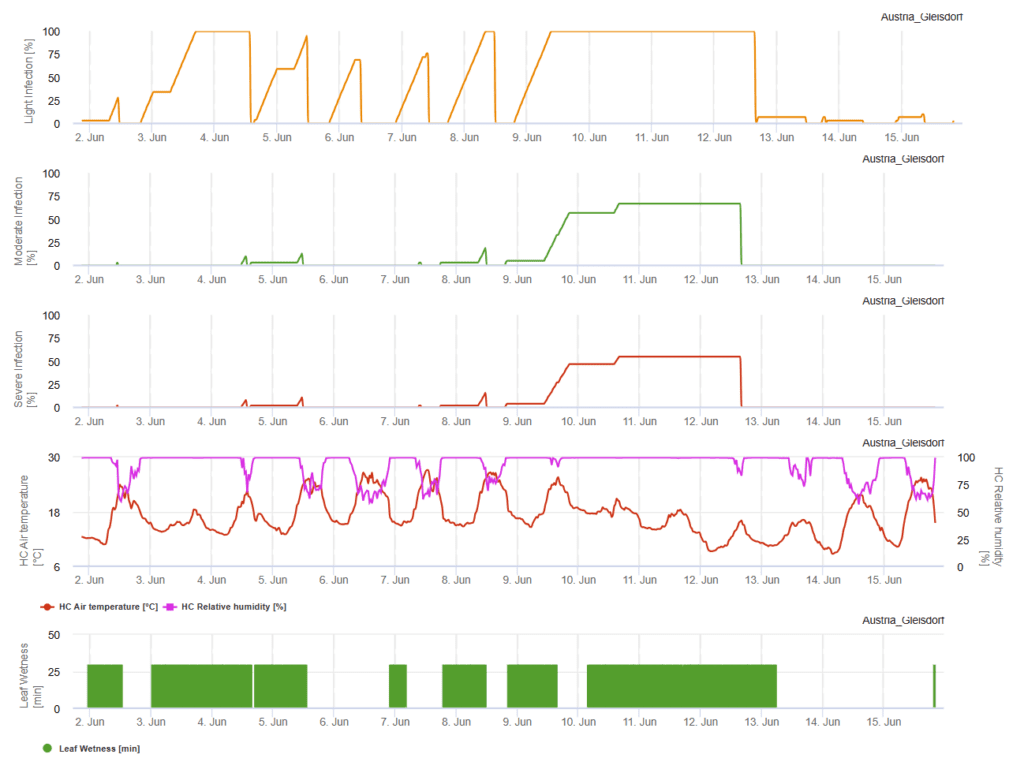
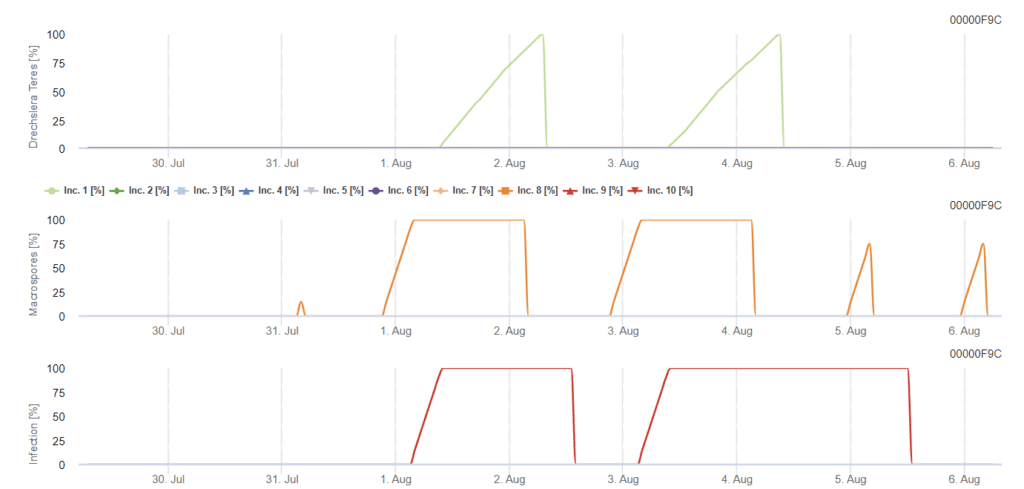
Das Primärinokulum entwickelt sich bei optimalen Temperaturen zwischen 15°C und 25°C, wobei das Optimum bei 20°C liegt. Bedingungen mit mehr als 6 Stunden Dunkelheit führen zu einem optimalen Wachstum der Konidien, wie in einer Sporulationskurve der Konidien dargestellt. Erreicht die Sporulationskurve den Wert 100%, sind die optimalen Bedingungen im Feld eingestellt.
Die weitere Ausbreitung erfolgt durch Wind oder Regen. Für die Infektion von Pflanzengeweben sind feuchte Bedingungen wie Blattnässe oder hohe relative Luftfeuchtigkeit für etwa 10 bis 30 Stunden bei optimalen Temperaturen von 15°C und 25°C erforderlich, wie in einem Infektionsdiagramm dargestellt. Wenn der Wert 100% erreicht wird, sind optimale Bedingungen für die Infektion im Feld gemessen worden. Sonnenlicht kann auch das Wachstum von Konidophoren fördern, die Konidien produzieren, wenn sich die Bedingungen zwischen feuchten und trockenen Perioden mit hoher Sonneneinstrahlung und niedriger relativer Luftfeuchtigkeit ändern und Wind die Entwicklung der Krankheit begünstigt.
Literatur
- Backes, A., Guerriero, G., Ait Barka, E., & Jacquard, C. (2021). Pyrenophora teres: Taxonomie, Morphologie, Interaktion mit Gerste und Art der Bekämpfung. Grenzgebiete der Pflanzenwissenschaften, 12, 614951.
- Liu, Z., Ellwood, S. R., Oliver, R. P., & Friesen, T. L. (2011). Pyrenophora teres: Profil eines zunehmend schädlichen Gerstenpathogens. Molekulare Pflanzenpathologie, 12(1), 1-19.
- Obst, A., & Paul, VH (1993). Krankheiten und Schädlinge des Getreides, Verlag Th. Mann, Gelsenkirchen-Buer.
Alles mitnehmen
Krankheitserreger
Die Krankheit "Take-all", verursacht durch Gaeumannomyces graminisist eine der verheerendsten Krankheiten im Getreideanbau. Der Name stammt von südaustralischen Landwirten, da die Krankheit so schädlich ist, dass sie kein Getreide mehr ernten können. Der Erreger schädigt das Wurzelsystem und den Stängel, verursacht Wasser- und Nährstoffmangel und führt schließlich zum Absterben der Pflanze.
Der Pilz überlebt in Form von Myzelien in Ernterückständen saprophytisch, und Fragmente im Boden können durch Wind, Wasser und Tiere transportiert werden. Die Primärinfektion erfolgt, sobald die Wurzeln der Sämlinge mit infizierten Abfällen in Berührung kommen, gefolgt von Hyphenwachstum und -ausbreitung. Sie durchdringen die Wurzelepidermis und dringen in die Wurzelrinde ein, kolonisieren und zerstören das Gewebe. Die Infektion schreitet aufwärts und abwärts fort. Die Sekundärinfektion erfolgt über Wurzel-zu-Wurzel-Kontakt, wobei stark infizierte Pflanzen in Flecken auftreten.
Symptome
Die Weizenkrankheit tritt typischerweise im Keimlings- und Bestockungsstadium auf und verursacht Symptome in der Nähe der Bodenoberfläche. Befallene Pflanzen können verkümmern, mit vergilbten Blättern und verfrüht reifenden Ähren, denen es an voll entwickelten Körnern fehlt. Die kreisförmigen, abgestorbenen Flecken, die von einigen Zentimetern bis zu mehreren Metern reichen, haben oft gelb-orange oder bronzefarbene Ränder und können in den Folgejahren an der gleichen Stelle wieder auftreten.
Zu den wichtigsten Symptomen gehören gebleichte weiße oder leere Ähren, geschwärzte Stängelansätze und dunkle, faulende Wurzeln mit kleinen schwarzen Läsionen, die sich ausdehnen. Schwer geschädigte Wurzeln sind brüchig, und auf dem basalen Stängel kann eine glänzende schwarze Verfärbung auftreten. Die Pflanzen können aufgrund ihres geschwächten Wurzelsystems leicht aus dem Boden gezogen werden. Die Krankheit kann einem Trockenstress ähneln, da sie die Wasserzufuhr zu den oberen Pflanzenteilen unterbricht und eine vorzeitige Fäulnis verursacht.
Modell FieldClimate
Alles mitnehmen
Modell Sensoren:
- Bodentemperatur
Das Take-All-Risikomodell verwendet die Tageslänge und die Bodentemperatur, um die risikoreichen Zeiträume zu bestimmen. Tage mit weniger als 13 Stunden Sonnenlicht und Bodentemperaturen zwischen 10°C und 20°C begünstigen die Krankheitsentwicklung.
Wenn der Risikowert 100% erreicht, sind auf dem Feld optimale Bedingungen für die Entwicklung des Erregers gegeben. Eine Fruchtfolge mit einem Abstand von mindestens 2 bis 3 Jahren zwischen anfälligen Getreidearten ist die wichtigste Schutzstrategie.
Literatur
- Cook, R. J. (2003). Take-all of wheat. Physiologische und molekulare Pflanzenpathologie, 62(2), 73-86.
- Palma-Guerrero, J., Chancellor, T., Spong, J., Canning, G., Hammond, J., McMillan, V. E., & Hammond-Kosack, K. E. (2021). Take-all-Krankheit: Neue Erkenntnisse über einen wichtigen Weizenwurzel-Pathogen. Trends in der Pflanzenwissenschaft, 26(8), 836-848. https://www.apsnet.org/edcenter/disandpath/fungalasco/pdlessons/Pages/Takeall.aspx
Fusarium-Krankheit
Krankheitserreger
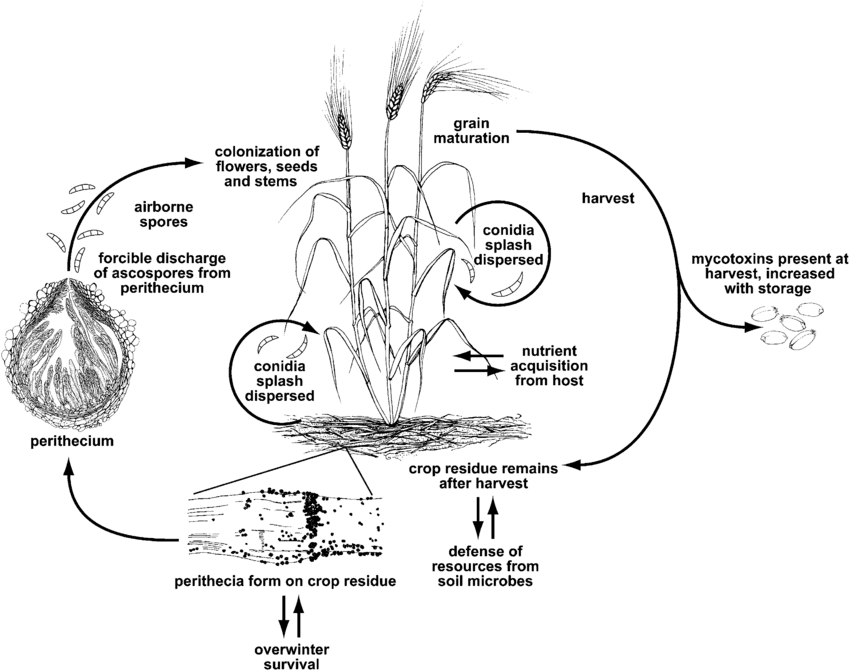
Fusarium-Kopffäule oder Schorf wird verursacht durch die Gattung Fusarium. Die häufigste Art ist Fusarium graminearum aber die am häufigsten vorkommenden Arten können je nach Region unterschiedlich sein.
F. graminearum kann Weizenpflanzen in jedem Wachstumsstadium infizieren. Er überlebt den Winter auf infizierten Ernterückständen, und im Frühjahr kommt es zur Primärinfektion, wenn Ascosporen aus Perithecien und Konidien auf Weizenspelzen oder Staubbeuteln verteilt werden. Befallene Blüten bilden schrumpelige oder verwelkte Körner, die oft als "Grabstein"-Körner bezeichnet werden. Selbst wenn die Körner nicht befallen erscheinen, können sie mit Mykotoxinen kontaminiert sein. Die Sekundärinfektion erfolgt über Konidien, aber Weizenepidemien hängen in erster Linie von der Menge des Primärinokulums und nicht von sekundären Quellen ab.
Fusarium-Kopffäule führt auch zur Anhäufung schädlicher Mykotoxine in den Pflanzen, die eine potenzielle Gefahr für Tiere darstellen. Diese Mykotoxine hemmen die pflanzlichen Abwehrmechanismen oder schützen den Pilz vor anderen Organismen. Das wichtigste Toxin ist Deoxynivalenol (DON), das die Proteinsynthese hemmt und die normale Zellfunktion stört. Bei Menschen, die DON-haltigen Weizen verzehrt haben, treten Symptome wie Übelkeit, Fieber oder Erbrechen auf.
Symptome

Bei Weizen und Hartweizen kann ein Teil oder der gesamte Kopf gebleicht erscheinen. Die teilweise weißen und grünen Köpfe sind ein diagnostisches Merkmal für die Krankheit bei Weizen. Der Pilz kann auch den Stängel befallen und eine braune bis violette Verfärbung verursachen. Bei feuchter Witterung sind auf den infizierten Ährchen und Spelzen häufig rosa bis lachsfarbene Sporenmassen zu sehen. Viele Körner sind verschrumpelt und leicht und werden aufgrund ihres kalkigen, leblosen Aussehens manchmal als Grabsteine" bezeichnet. Unter günstigen Bedingungen kann sich die Infektion auf benachbarte Ährchen ausbreiten und die gesamte Ähre, einschließlich der Spindel und des Stiels, befallen. Die Körner können bei normaler Größe ein stumpfes Aussehen und eine rosa Verfärbung aufweisen, wenn die Infektion erst spät im Entwicklungsstadium aufgetreten ist.
Bei Gerste bleichen die infizierten Ährchen aus und zeigen ein wassergetränktes Aussehen. Auch die Körner können eine Verfärbung aufweisen, und gelegentlich sind bei feuchten Bedingungen lachsfarbene Sporenmassen auf Ährchen und Spelzen zu sehen.
FieldClimate-Modelle
Die Schätzung des FHB-Gehalts eines Feldes basiert auf der Zählung der befleckten Köpfe oder Körner. Die farbige visuelle Skala zur Einschätzung des FHB-Schweregrads bei Weizen ist beim NDSU Extension Service erhältlich (Veröffentlichung PP-1095): https://library.ndsu.edu/ir/bitstream/handle/10365/9187/PP1095_1998.pdf?sequence=1&isAllowed=y.
Fusarium Head Blight Infektionsmodell (Fusarium Head Blight Risiko)
Benötigte Sensoren:
- Lufttemperatur
- Relative Luftfeuchtigkeit
- Blattnässe
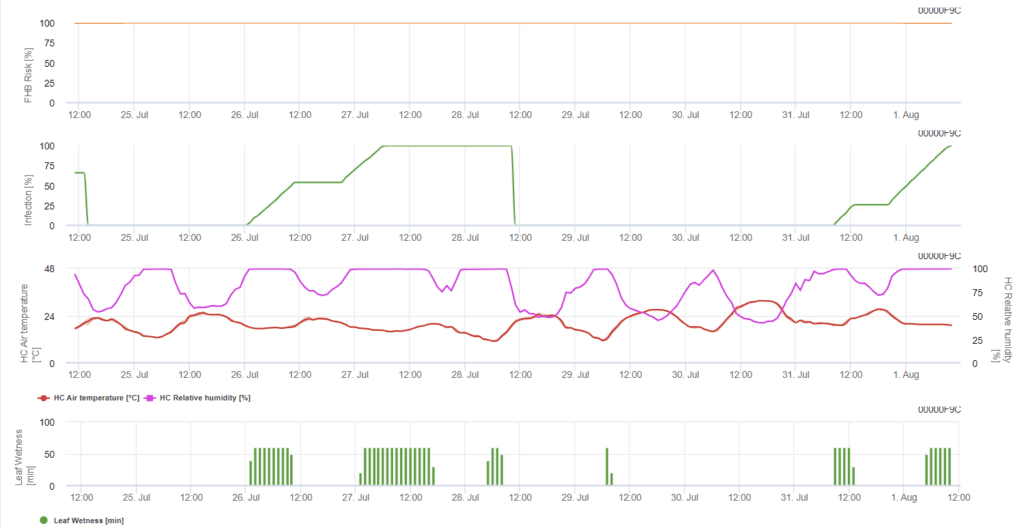
Das Modell bestimmt die risikoreichen Zeiträume für eine Infektion. Immer wenn die 100%-Infektion erreicht ist, ist das Risiko sehr hoch, und die Bedingungen für den Pilz waren günstig für eine Infektion. Das Wissen des Landwirts über das Entwicklungsstadium der verschiedenen Weizensorten gibt ihm die Möglichkeit, eine kurative Spritzung unmittelbar nach der Infektion durchzuführen.
Die pilzlichen Erreger der Fusarium-Kopffäule an Weizen werden durch warme Temperaturen von 20 °C bis 30 °C und lange Feuchtigkeitsperioden begünstigt. Mehrtägige Blattnässeperioden führen zu früh sichtbaren Symptomen. Symptome können auch nach einer langen Latenzzeit auftreten, wenn der Infektion eine Blattnässeperiode von 18 Stunden oder noch kürzer und ein künstliches Inokulum bei Temperaturen von 15°C folgt.
Wir haben alle in der Literatur gefundenen Temperatur- und Feuchtigkeitskombinationen zusammengefasst und beschlossen, auf Fusarium-Kopffäule-Infektionen hinzuweisen, wenn Temperatur und Blattnässeperiode oder Perioden mit mehr als 85% relativer Feuchtigkeit die in der folgenden Grafik dargestellten Werte überschreiten. Die Berechnung des Fortschrittswertes folgt der Beziehung zwischen der Dauer der Feuchtigkeit und der Temperatur.
Fusarium-Mykotoxin-Warnmodell (Fusarium Head Blight)
Benötigte Sensoren:
- Lufttemperatur
- Relative Luftfeuchtigkeit
- Blattnässe
- Niederschlag
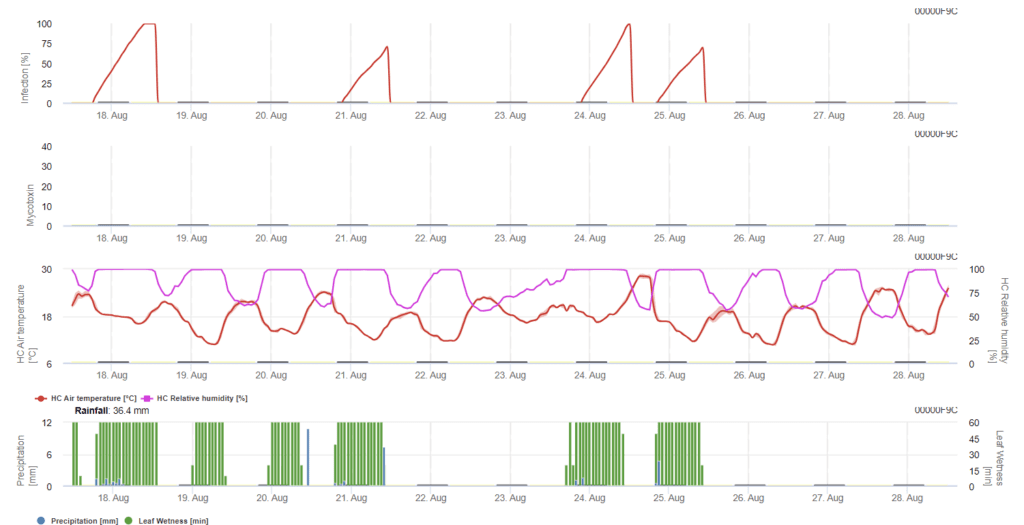
In diesem Modell wird die Infektion des FHB durch Niederschlag (2 mm erforderlich), relative Luftfeuchtigkeit (über 85%) oder Blattnässe, Temperatur während des Prozesses berechnet. Wenn die Infektion 100% erreicht, sind optimale Bedingungen für den Pilzerreger gegeben. Des Weiteren berechnet das Modell das FHB-Mykotoxinrisiko.
Infektionsversuche mit längeren Blattnässeperioden von Fusarium-Kopffäule führen zu hohen Mykotoxingehalten. Aufgrund dieser Informationen wird davon ausgegangen, dass eine Blattnässeperiode von 48 Stunden oder mehr während der Stadien 61 und 69 ein hohes Risiko für Mykotoxine darstellt.
Die Erfahrungen, die bei der Analyse von DON in kommerziell angebautem Weizen gemacht wurden, haben gezeigt, dass ausreichend lange Blattnässeperioden für eine Infektion nach einer Erstinfektion in den Stadien 61 bis 69 die DON-Werte erhöhen können. Bei längeren Blattnässeperioden können die Mykotoxine bis zum Stadium 85 ansteigen.
- BBCH-Stadium 61: Beginn der Blüte; erste Antheren sichtbar
- BBCH-Stadium 69: Ende der Blüte; alle Ährchen haben die Blüte abgeschlossen, aber einige vertrocknete Antheren können zurückbleiben
- BBCH-Stadium 85: In der Mitte der Reifung; weicher Teig mit weichem, aber trockenem Korngehalt, Fingernagelabdruck nicht gehalten
Das Modell akkumuliert die Risikozahl proportional zum Infektionsfortschritt für jede erfolgreiche Infektionsperiode über den für die Berechnung gewählten Zeitraum. Sechs abgeschlossene Infektionen würden zu einem Risiko von 100% führen. Normalerweise ist der Zeitraum der Blattnässe, der zu einer Fusarieninfektion führt, länger als das erforderliche Minimum. Daher werden die meisten Fusarieninfektionen zu einer Risikoerhöhung von mehr als 17% führen.
Der Wert des Mykotoxinrisikos hängt von der Feldgeschichte ab. Weizen, der nach Direktsaat angebaut wird, kann nur ein geringes Risiko tragen, wenn er nicht in der optimalen Situation gespritzt wird. Bei ungespritztem Weizen müssen wir mit erhöhten DON-Werten nach 35% des Risikos rechnen. Weizen nach ungespritztem Weizen, der auf eine andere Kultur folgt, kann ein höheres Risiko von 50% bergen. Bei Weizen nach Weizen mit Bodenbearbeitung kann das Risiko auf bis zu 70% steigen. Erstjähriger Weizen sollte auf DON getestet werden, wenn das Risiko 100% erreicht.
Literatur
- https://www.fao.org/4/y4011e/y4011e0j.htm
- https://scabusa.org/pdfs/NDSU_PP-804_FHB-Small-Grains.pdf
- Lancashire, P. D., Bleiholder, H., Boom, T. V. D., Langelüddeke, P., Stauss, R., Weber, E., & Witzenberger, A. (1991). Ein einheitlicher Dezimalcode für Wachstumsstadien von Kulturpflanzen und Unkräutern. Annals of Applied Biology, 119(3), 561-601.
- Trail, F. (2009). Für gefärbte Wellen von Getreide: Fusarium graminearum in der Postgenomik-Ära. Pflanzenphysiologie, 149(1), 103-110.
- Schumann, G. L. (2010). Der Lehrer für Pflanzengesundheit| Band: 10| Jahr: 2010| Artikelart: Unterrichtspläne. Pflanzengesundheit, 10.
Gerste gestreift
Krankheitserreger
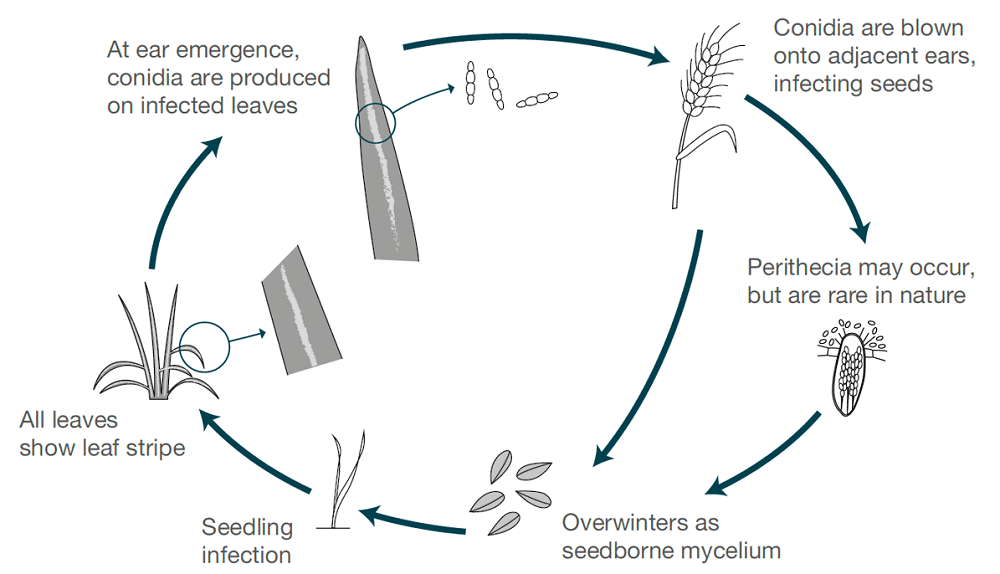
Gerstenstreifen werden verursacht durch Pyrenophora graminea (Drechslera graminea)ist ein samenbürtiger Erreger, der in der Epidermis eines infizierten Samens überlebt. Der Pilz infiziert die Sämlinge unter kühlen, feuchten Bedingungen. Der Pilz wächst systemisch in der Pflanze, infiziert die gesamte Pflanze, produziert Toxine, tötet Zellen ab und verfärbt das Blattgewebe zwischen den Adern, was zu gestreiften Läsionen führt. Die Streifenkrankheit tritt bei Wintergerste häufiger auf als bei Sommergerste.
Bei nassen oder feuchten Bedingungen werden die Sporen auf der Blattoberfläche produziert, wenn gesunde Pflanzenstacheln blühen. Die Sporen werden durch den Wind auf diese sich entwickelnden Ähren verteilt, keimen und verursachen Infektionen. Die Kerne sind in der frühen Entwicklungsphase am anfälligsten. In jeder Saison findet nur ein Zyklus der Infektion und Sporenproduktion statt.
Symptome

Die Symptome treten vor allem in der Phase des Ährenschiebens auf.
Blassgrüne bis gelbe Streifen erscheinen zunächst am unteren Teil des Blattes und der Blattscheide. Diese Streifen färben sich allmählich braun bis dunkelbraun, gefolgt von einer Austrocknung und Aufspaltung der Blattspreite. Sie dehnen sich auf die gesamte Länge des Blattes aus, werden nekrotisch und verschmelzen miteinander, was schließlich zum Absterben der Pflanze führt.
Die Pflanzen können verkrüppelt erscheinen, nur wenige Triebe bilden und in schweren Fällen keinen Kopf oder Samen produzieren. Auch die Ährenlänge kann aufgrund schlecht entwickelter brauner Körner reduziert sein.
Modell FieldClimate
Pyrenophora graminea Modell
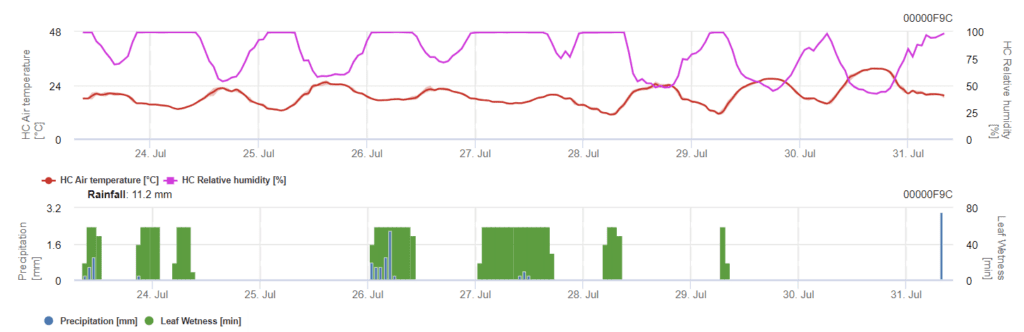
Benötigte Sensoren:
- Lufttemperatur
- Relative Luftfeuchtigkeit
- Blattnässe
- Niederschlag
Das Modell ist in zwei Stufen unterteilt. Die erste Stufe sind die risikoreichen Perioden während der Notzeiten der Pflanze, die frühen Stadien. Das zweite Stadium ist die Blütezeit und die Entwicklung des Gerstenkopfes. Wenn die Infektion 100% erreicht, sind auf dem Feld optimale Bedingungen geschaffen worden, damit der Pilz das Pflanzengewebe infizieren und systematisch darin wachsen kann.
Literatur
- Richardson, M. J. (1996). Saatgut-Mykologie. Mykologische Forschung, 100(4), 385-392. https://ahdb.org.uk/knowledge-library/barley-leaf-stripe-life-cycle-and-disease-symptoms https://plantwiseplusknowledgebank.org/doi/full/10.1079/pwkb.species.46115
Septoria
Krankheitserreger
Es gibt zwei wichtige Septoria-Krankheiten bei Weizen - Septoria tritici blotch, verursacht durch Septoria tritici und Septoria nodorum-Fleck, verursacht durch Septoria nodorum.
Septoria tritici überlebt auf infizierten Ernterückständen während des Sommers und beginnt im Herbst, Weizenpflanzen zu infizieren. Der Pilz gedeiht unter kühlen und feuchten Bedingungen. Er durchläuft zwei Stadien - eine latente Phase und eine nekrotische Phase. In der Latenzphase beimpft der Pilz neues Pflanzengewebe, dringt durch die Spaltöffnungen ein und kolonisiert, wobei er interzellulär im Pflanzengewebe wächst. S. tritici benötigt keine physischen Ernährungsstrukturen, sondern ernährt sich selbst, indem es Nährstoffe aus den Wirtszellen extrahiert, die ihre strukturelle Integrität verloren haben. Die Pflanzen können überempfindlich reagieren, und als Reaktion auf die Infektion können sich an den betroffenen Geweben nekrotische Läsionen bilden.
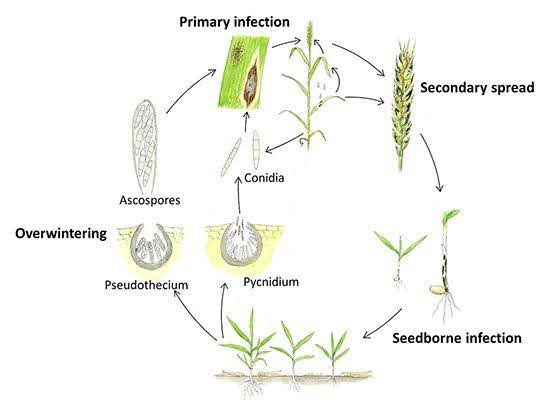
Septoria nodorum überlebt den Sommer als schlafende Myzelien, Pyknidien und Pseudothezien auf Ernterückständen. Die Infektion beginnt in der Regel im Herbst, wenn Pyknidiosporen aus Pyknidien und Ascosporen aus Pseudothezien durch Wind und Regen verbreitet werden und die Primärinfektion einleiten. Diese Sporen durchdringen die Blattkutikula, und nach der Infektion kommt es zur Bildung von Pyknidien. Die Sekundärinfektion erfolgt durch die Bildung von Pyknidiensporen, die von den unteren Blättern auf die oberen Blätter und Spelzen übertragen werden. Der Erreger produziert auch Toxine, die zur Entwicklung der Krankheit beitragen.
Symptome
Septoria tritici-Fleck
Im Herbst, Septoria tritici Die Symptome erscheinen zunächst als kleine gelbe Flecken auf den Blättern, die winzige schwarze Sprenkel enthalten, bei denen es sich um Pilzfruchtkörper handelt. Die Läsionen sind unregelmäßig geformt, von elliptisch bis lang und schmal, vergrößern sich und werden mit zunehmender Reife braun bis rötlichbraun. Die Krankheit beginnt in der Regel an den unteren Blättern und wandert allmählich nach oben, bis sie schließlich das Fahnenblatt befällt. Bei feuchter Witterung kann der Pilz auf die Weizenköpfe übergreifen und braune Läsionen an den Spelzen und Grannen verursachen, die als Spelzenfleck bekannt sind. Der Septoria tritici-Fleck kann mit anderen Weizenkrankheiten verwechselt werden. Das Vorhandensein von schwarzen Pilzkörpern ist jedoch ein Hauptmerkmal von S. tritici. Obwohl Septoria nodorum unter feuchten Bedingungen auch braune Fruchtkörper produzieren kann, unterscheiden sie sich in Farbe und Größe, wobei Septoria tritici die Fruchtkörper sind größer.
Septoria-nodorum-Fleck
Septoria nodorum Die Symptome treten zuerst auf den oberen Blättern auf. Zunächst erscheinen auf den Blättern dunkelbraune Flecken mit einem gelben Heiligenschein. Das Verbrennen der Blattspitzen ist ein weiteres erstes Anzeichen. Die Läsionen dehnen sich aus und werden mit zunehmender Reife nekrotisch mit einem dunkelbraunen Zentrum. In den Läsionen sind winzige dunkelbraune Strukturen zu sehen, bei denen es sich um Fruchtkörper handelt. Die aus den Fruchtkörpern freigesetzten Konidien sehen wie weiße bis rosafarbene Massen aus. Stark befallene Blätter können vollständig mit Läsionen bedeckt sein, was schließlich zum Absterben des Blattgewebes führt. Der Pilz kann auch Spelzen und Grannen befallen: Es entstehen ähnliche braune Läsionen, und die Krankheit schreitet nach unten fort.
Modell FieldClimate
Septoria-Infektionen sind bei niedrigen Temperaturen möglich, wobei Temperaturen unter 7°C innerhalb von 2 Tagen nicht zu einer Infektion führen können. Das Temperaturoptimum der Krankheit wird im Bereich von 16 bis 21°C erreicht. Infektionen sind innerhalb einer Periode hoher relativer Luftfeuchtigkeit oder Blattnässe von 14 Stunden oder länger möglich.
Septoria tritici Modell
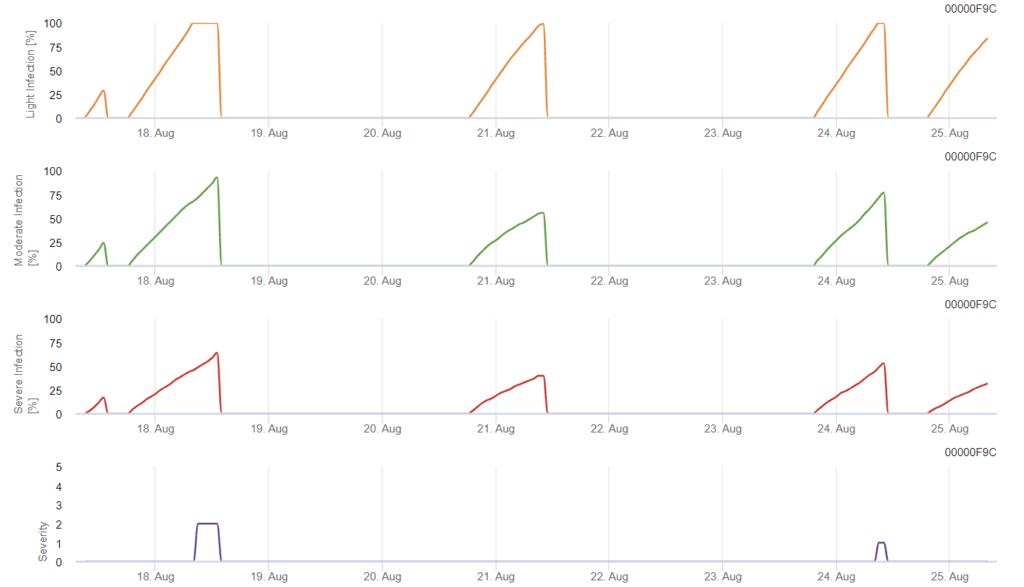
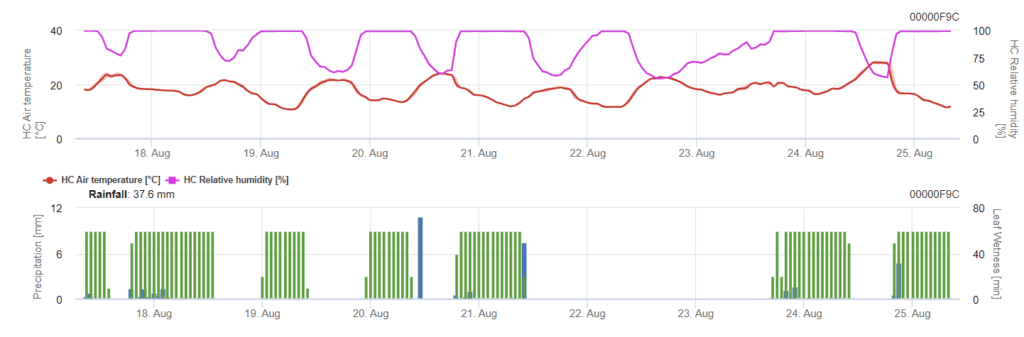
Die Infektion beginnt nach einem Regen von 0,5 mm. Die optimalen Temperaturen für Septoria-Infektionen liegen bei 16°C bis 21°C und Blattnässe oder hoher relativer Luftfeuchtigkeit über 14 Stunden. Septoria tritici wird in drei Schweregrade eingeteilt. Außerdem legen wir Schweregrade fest, die die Bewertung des Infektionsdrucks zwischen den BBCH-Stadien 10 bis 32 bei Weizen unterstützen.
- BBCH-Stadium 10: Blattentwicklung; erstes Blatt durch Koleoptil
- BBCH-Stadium 32: Halmverlängerung; Knoten 2 mindestens 2 cm über Knoten 1
- BBCH-Stadium 51: Erscheinen des Blütenstandes und Austrieb; Beginn des Austriebs, wenn die Spitze des Blütenstandes aus der Blattscheide austritt und das erste Ährchen gerade sichtbar ist.
Wir haben beschlossen, kein Modell für die Pyknidienbildung zu verwenden. Als Voraussetzung für die Bildung von Pyknidien wird ein Zeitraum mit einer relativen Luftfeuchtigkeit von mehr als 85% angenommen. Die Lebensdauer der Pyknidien beträgt 24 Stunden. In allen Klimazonen, in denen der Pilz eine Chance hat, sich zu infizieren, werden wir fast jeden Tag um den Sonnenaufgang herum zwei Stunden finden, die diese Bedingung erfüllen.
Bewertung des Schweregrads der Infektion
Zur Bewertung der Septoria tritici Infektionsdruck zwischen den Stufen 10 und 32 und zwischen 32 und 51 müssen wir die Schwere der Infektionen auf der Grundlage der klimatischen Bedingungen bewerten. Der Schweregrad der Infektion wird auf einer Skala von 1 bis 5 bewertet:
- 1: schwache Infektion mit weniger als 5 mm Regen
- 2: Schwache Infektion mit mehr als 5 mm Regen
- 3: mäßige Infektion mit weniger als 5 mm Regen
- 4: mäßige Infektion mit mehr als 5 mm Regen/ schwere Infektion mit weniger als 5 mm Regen
- 5: schwere Infektion mit mehr als 5 mm Regen
Bewertung des Krankheitsdrucks
Es gibt drei Faktoren für den Krankheitsdruck auf dem Feld - Klima, Feldgeschichte und die Anfälligkeit der angebauten Sorte. Wenn wir die Krankheitsschwerewerte von Stadium 10 bis Stadium 32 auf den Wert 4 akkumulieren können, können wir einen schwachen Krankheitsdruck durch das Klima erwarten. Erreicht dieser Wert den Wert 6, ist mit einem mäßigen Krankheitsdruck zu rechnen, und wenn er den Wert 10 erreicht, mit einem höheren Krankheitsdruck durch das Klima.
Die Kenntnis der Anfälligkeit der Sorte und der Feldgeschichte führt dazu, dass wir bei einem schwachen oder mäßigen Krankheitsdruck in der Situation spritzen oder nicht. Ein kumulierter Wert von 10 kann in jedem Fall zu einer Spritzung im Stadium 32 führen.
Die Entscheidung, in einem späteren Stadium zu spritzen, hängt von den klimatischen Bedingungen im Frühjahr ab. Wenn wir die Schweregrade von Stadium 10 bis zu einem Wert von 6 akkumulieren können, können wir einen schwachen Krankheitsdruck erwarten. Erreicht dieser Wert 10, ist mit einem mäßigen Krankheitsdruck zu rechnen, und wenn dieser Wert 15 erreicht, ist aufgrund der klimatischen Bedingungen ein hoher Krankheitsdruck zu erwarten.
In FieldClimate wird die Septoria tritici Schweregrad zusammen mit den drei verschiedenen Infektionsschweregraden dargestellt. Aufgrund von Niederschlägen und langer Blattnässe sind die Bedingungen für eine schwere Infektion mit S. tritici erfüllt. Die Schweregrade erreichen den höchsten Wert von 5, was bedeutet, dass ein hohes Infektionsrisiko besteht.
Septoria nodorum Modell
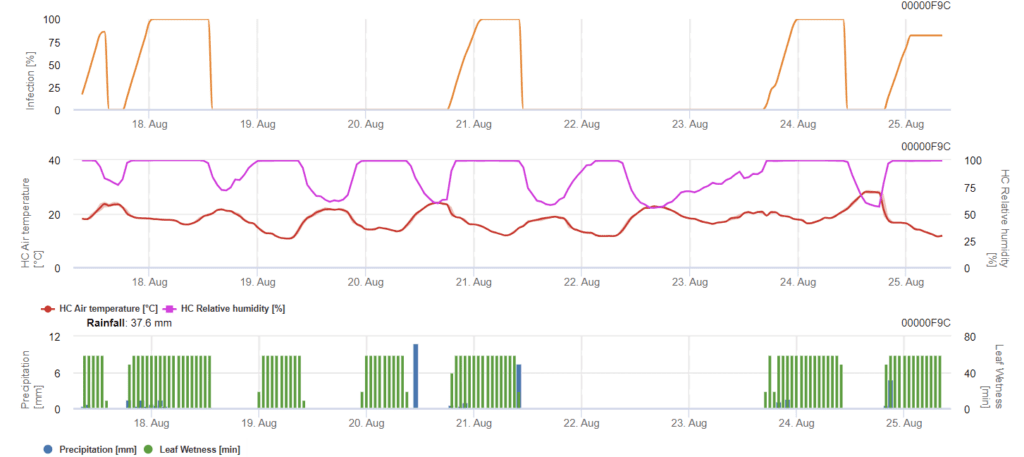
Septoria nodorumDie Infektionsbiologie unterscheidet sich in gewissem Maße von Septoria tritici aber der Unterschied ist nicht groß genug für ein eigenes Modell. Wir schlagen daher vor, das Tritici-Modell für den gesamten Septoria-Krankheitskomplex zu verwenden. In Gebieten mit hohem Druck von S. nodorumInfektionen, die als schwach mit einem Schweregrad von 2 eingestuft werden, sollten ernster behandelt werden als in anderen Bereichen.
Die Septoria nodorum Das Modell berechnet das Risiko der Krankheit. Pflanzenschutzmaßnahmen sollten in Betracht gezogen werden, wenn das Risiko 80% erreicht. Wenn das Risiko 100% beträgt und eine Infektion bereits festgestellt wurde, sollten systemische Pflanzenschutzmaßnahmen (kurative Anwendungen) ergriffen werden.
Literatur
- Brennan, C. J., Benbow, H. R., Mullins, E., & Doohan, F. M. (2019). A review of the known unknowns in the early stages of septoria tritici blotch disease of wheat. Pflanzenpathologie, 68(8), 1427-1438.
- De Wolf, E. D. (2008). Septoria tritici blotch. Mehra, L. K., Adhikari, U., Ojiambo, P. S., & Cowger, C. (2019). Septoria nodorum-Fleckenkrankheit bei Weizen. Der Ausbilder für Pflanzengesundheit.
- Solomon, P. S., Lowe, R. G., TAN, K. C., Waters, O. D., & Oliver, R. P. (2006). Stagonospora nodorum: Ursache der Stagonospora nodorum-Fleckenkrankheit bei Weizen. Molekulare Pflanzenpathologie, 7(3), 147-156.
Blattfleck
Krankheitserreger
Die Blattfleckenkrankheit wird verursacht durch Rynchosporium secalis.
Die Primärinfektion erfolgt durch Ascosporen oder Konidien auf Pflanzenresten. Diese Sporen werden durch Wind und Regen verbreitet, keimen, und wenn die Epidermis- und Mesophyllzellen nach einer Infektion zusammenbrechen, werden die Symptome sichtbar. Die Sekundärinfektion erfolgt durch Konidien von infizierten Blättern. Unter feuchten Bedingungen keimen die Konidien auf der Blattoberfläche und bilden Hyphen, die die Kutikula direkt über den Epidermiszellen durchdringen. Das anschließende Pilzwachstum beschränkt sich auf den subkutikulären Bereich der Epidermis.
Symptome
R. secalis kann jeden Teil der Blätter befallen. Das Hauptmerkmal sind unregelmäßig geformte Flecken, und die Infektion beginnt von der Unterseite bis zu den oberen Blättern. Die Flecken erscheinen zunächst als wassergetränkte Bereiche. Wenn die Krankheit fortschreitet, werden sie in der Mitte durch Sporenbildung gräulich und haben einen braunen Rand. Nekrose und Chlorose können folgen. Die Flecken wachsen zusammen und zerstören die gesamten Blätter.
Modell FieldClimate
Blattfleckenkrankheit Rynchosporium Modell
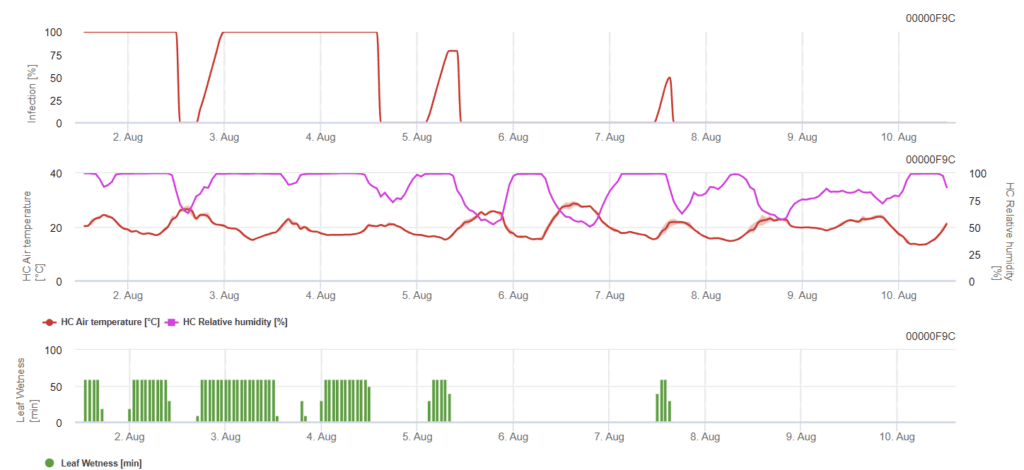
Benötigte Sensoren:
- Lufttemperatur
- Relative Luftfeuchtigkeit
- Blattnässe
Für eine Infektion sind je nach Temperatur mindestens 7 bis 15 Stunden Bleinässe erforderlich (optimal bei 20'C). Wenn das Diagramm den Wert 100% erreicht, bedeutet dies, dass die optimalen Bedingungen im Feld ermittelt wurden.
Literatur
- Brooks, F. T. (1928). Beobachtungen über Rhynchosporium secalis (Oud.) Davis, Blattfleckenkrankheit von Gerste und Roggen. Neuer Phytologe, 27(4), 215-219.
- Fowler, A. M., & Owen, H. (1971). Studies on leaf blotch of barley (Rhynchosporium secalis). Transaktionen der Britischen Mykologischen Gesellschaft, 56(1), 137-152.
- Zhan, J., Fitt, B. D., Pinnschmidt, H. O., Oxley, S. J. P., & Newton, A. C. (2008). Resistenz, Epidemiologie und nachhaltiges Management von Rhynchosporium secalis-Populationen auf Gerste. Pflanzenpathologie, 57(1), 1-14.
Ramularia-Blattfleck
Krankheitserreger
Ramularia collo-cygni, der Erreger der Ramularia-Blattfleckenkrankheit an Gerste, verbreitet sich hauptsächlich durch ungeschlechtliche Vermehrung über Konidien, die für die Keimung und frühe Entwicklung Feuchtigkeit benötigen. Nach der Keimung auf der Blattoberfläche dringt der Pilz durch die Spaltöffnungen in das Blatt ein und kolonisiert das Gewebe interzellulär. Befallene Gerstenpflanzen können anfangs keine Symptome zeigen, aber Schäden treten typischerweise nach der Blüte auf.
Der Lebenszyklus von R. collo-cygni ist nicht vollständig geklärt, aber es handelt sich um eine vertikale Übertragung durch infiziertes Saatgut, die es dem Erreger ermöglicht, zwischen den Wachstumsperioden zu überleben. Über die Luft übertragene Konidien tragen ebenfalls zur sekundären Ausbreitung bei und lösen unter günstigen Bedingungen neue Infektionen aus. Während Samen der primäre Überwinterungsmechanismus sind, spielt die Rolle von Zwischenwirten und einer sekundären Pilzstruktur namens Asteromella bleibt ungewiss und wird noch untersucht.
Symptome

Die Symptome treten im Allgemeinen nach der Blüte auf beiden Seiten der Blätter auf, sind aber häufiger auf den oberen Blättern zu finden. Die ersten Symptome erscheinen als gelbe bis braune Flecken an den Blattadern, umgeben von einem chlorotischen Lichthof. Sobald die Blattflecken auftauchen, wird das Blatt chlorotisch und nekrotisch, typischerweise beginnend an der Blattspitze und den Blatträndern. Benachbarte Flecken können ineinander übergehen und größere dunkle Bereiche bilden. Es können auch kleine punktförmige Flecken beobachtet werden. Obwohl die Symptome der Ramularia-Blattfleckenkrankheit mit anderen Krankheiten verwechselt werden können, ist das Hauptmerkmal, dass die Blattflecken auf die Blattadern begrenzt sind.
Es gibt die sogenannten 5R zur Unterscheidung von Ramularia-Blattflecken:
- Umrandet mit einem gelben Chlorose-Rand
- Rechteckige Form
- Begrenzt durch die Blattadern
- Rötlich-braune Färbung
- Mitten durch das Blatt
FieldClimate Modell
Ramularia-Modell
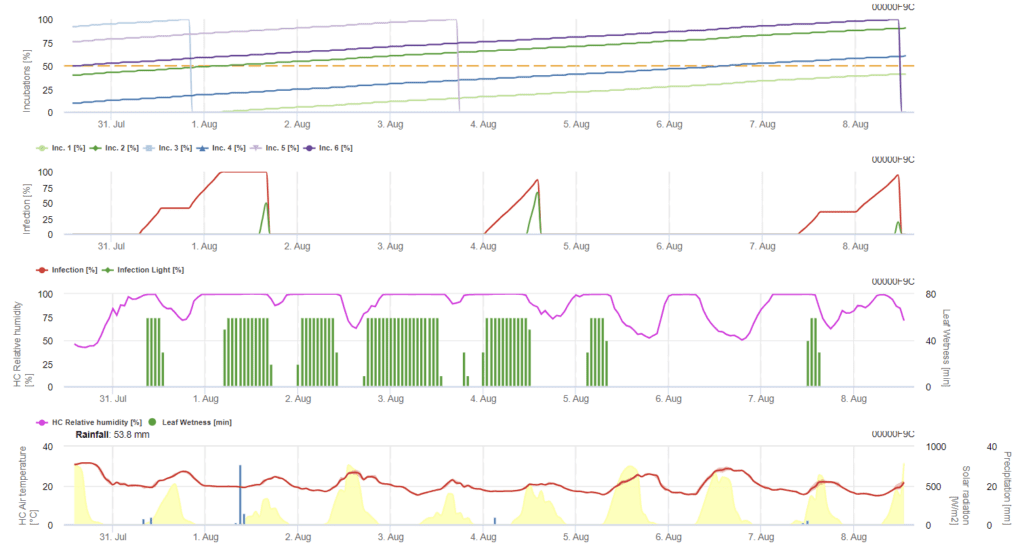
Die Ramularia-Infektion auf Gerste wird hauptsächlich durch feuchte Bedingungen verursacht. Daher beginnen wir die Berechnung mit einem Regenereignis, gefolgt von einer Blattnässe oder einer relativen Luftfeuchtigkeit von mehr als 85%.
Es werden zwei Arten einer Infektion beschrieben:
- Infektion: einmal, wenn feuchte Bedingungen ein Infektionsereignis nur begünstigen
- Infektion: einmal, wenn eine Globalstrahlung erforderlich ist, um ein Infektionsereignis zu beenden
Sobald eine Infektion von 100% erreicht wird, beginnt das Modell, die Inkubationszeit zu bestimmen. Wenn die Inkubationszeit 50% erreicht, wird empfohlen, das Feld auf neues Inokulum zu kontrollieren, und wenn sie 100% erreicht, werden nekrotische Läsionen auf den Blättern vorhergesagt.
Literatur
- Havis, N. D., Brown, J. K., Clemente, G., Frei, P., Jedryczka, M., Kaczmarek, J., ... & Hess, M. (2015). Ramularia collo-cygni-ein neu aufkommender Krankheitserreger von Gerstenkulturen. Phytopathologie, 105(7), 895-904.
- Huss, H. (2002, April). Die Biologie von Ramularia collo-cygni. In Proc. Second Int. Workshop Barley Leaf Blights. Aleppo, Syrien (S. 321-328).
- Walters, D. R., Havis, N. D., & Oxley, S. J. (2008). Ramularia collo-cygni: The biology of an emerging pathogen of barley. FEMS Microbiology Letters, 279(1), 1-7. https://grdc.com.au/__data/assets/pdf_file/0025/443509/GRDC_FS2103_Ramularia_03.pdf
Rhizoctonia solani
Krankheitserreger
Die Rhizoctonia-Wurzelfäule bei Weizen wird verursacht durch Rhizoctonia solani. Der Erreger kann viele Jahre lang als Sklerotien im Boden überleben. In einigen Fällen überlebt er auch in Form von Myzelien auf Pflanzenresten. Sobald die Temperatur steigt, werden die Sklerotien aktiv und bilden eine Masse von Hyphen, die eine Infektion durch Anheften an die Wurzeln ermöglichen. Das Myzel bildet so genannte "Infektionspolster", und der Pilz dringt in das Wurzelgewebe ein und besiedelt es. Die Wurzelinfektion schwächt die Sämlinge, was zu schlechtem Wachstum führt, und verringert die Fähigkeit, Wasser und Nährstoffe zu den oberirdischen Pflanzengeweben zu transportieren, was schließlich zum Absterben der Pflanze führt.
Symptome
Schon früh treten kahle Stellen auf, die von einigen Zentimetern bis zu mehreren Metern Durchmesser reichen können. Diese kahlen Stellen sind oft mit verkümmerten Pflanzen verbunden, die vergilben, welken oder sogar eine violette Färbung aufweisen können. Befallene Pflanzen können stark verkrüppelt sein und Anzeichen von Trockenstress oder Nährstoffmangel aufweisen, was in einigen Fällen zu einem vorzeitigen Absterben führen kann.
An Stängeln und Wurzeln unterhalb der Erdoberfläche bilden sich rötlich-braune Läsionen, die mit fortschreitender Krankheit immer tiefer werden. Die Wurzelfäule kann die Knöllchenbildung beeinträchtigen und dazu führen, dass die Wurzelrinde leicht brüchig wird, was zu braunen Speerspitzen führt.
Modell FieldClimate
Rhizoctonia solani Risikomodell
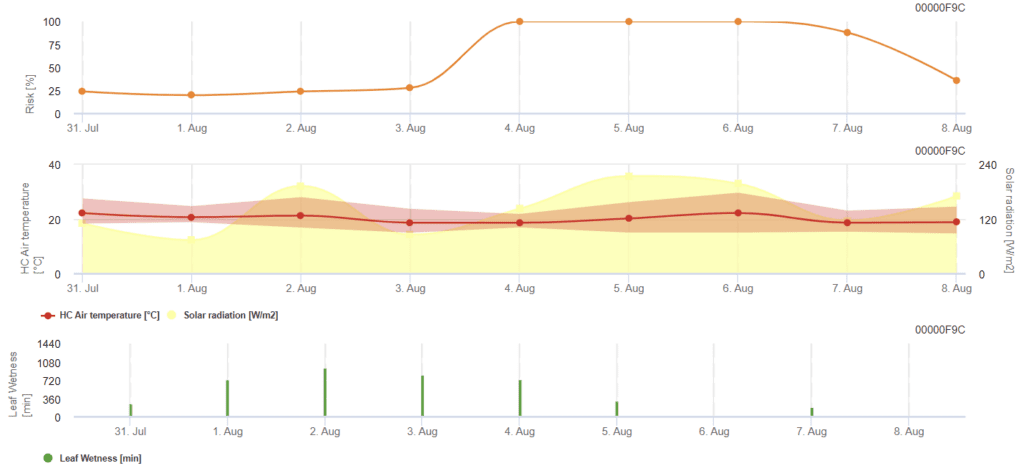
Benötigte Sensoren:
- Lufttemperatur
- Sonneneinstrahlung
- Blattnässe
Das Modell berechnet risikoreiche Zeiträume von Rhizoctonia solani durch Überprüfung der Bedingungen in den letzten 120 Stunden. Daraus ergibt sich ein Risikowert von 0 bis 100, der auf günstige Bedingungen für die Krankheit hinweist.
Bei geringem Risiko sind keine Spritzungen erforderlich. In Perioden mit mäßigem Risiko kann das Spritzintervall verlängert werden, und in Perioden mit hohem Risiko muss es möglicherweise verkürzt werden, oder es wird der Einsatz wirksamerer Mittel empfohlen.
Bei fortlaufender Blattnässe akkumuliert es minütlich temperaturabhängige Werte:
- 12 °C bis 15 °C: Akkumulation von 1 pro Minute
- 16 °C bis 17 °C: Akkumulation von 2 pro Minute
- 18°C und mehr: Akkumulation von 4 pro Minute
Am Ende der Blattnässeperioden wertet sie die kumulierten Werte aus:
- Werte > 4096: Risikoerhöhung um 64 Punkte und Subtraktion von 4096 vom Wert
- Restwerte > 2048: Risikoerhöhung um 16 Punkte und Subtraktion von 2048 vom Wert
- Rückstandswerte >1024: Risiko erhöht sich um 4 und Subtraktion von 1024 vom Wert
Wenn die Globalstrahlung konsekutiv höher als 800 W/m² ist, akkumuliert es die Zeit in Minuten und wertet die Werte aus, wenn die Strahlung niedriger wird:
- Wert > 512: Risiko - 32 Punkte, Wert - 512
- Wert > 256: Risiko - 8 Punkte, Wert - 256
- Wert > 128: Risiko - 2 Punkte, Wert - 128
Literatur
- https://cropprotectionnetwork.org/encyclopedia/rhizoctonia-root-rot-of-wheat#:~:text=It%20is%20caused%20by%20Rhizoctonia,result%20in%20premature%20plant%20death.
- https://ahdb.org.uk/knowledge-library/rhizoctonia-stunt-symptoms-and-risk-in-cereals
- https://cropwatch.unl.edu/rhizoctonia-root-rot#:~:text=Disease%20Symptoms&text=These%20reddish%20brown%20lesions%20may,uneven%20because%20of%20stunted%20plants.
- https://extensionaus.com.au/FieldCropDiseasesVic/docs/identification-management-of-field-crop-diseases-in-victoria/soil-borne-diseases/rhizoctonia-root-rot/
- https://www.florimond-desprez.com/es/wp-content/uploads/sites/6/2015/11/rhizoctonia_eng.pdf
Echter Mehltau
Krankheitserreger
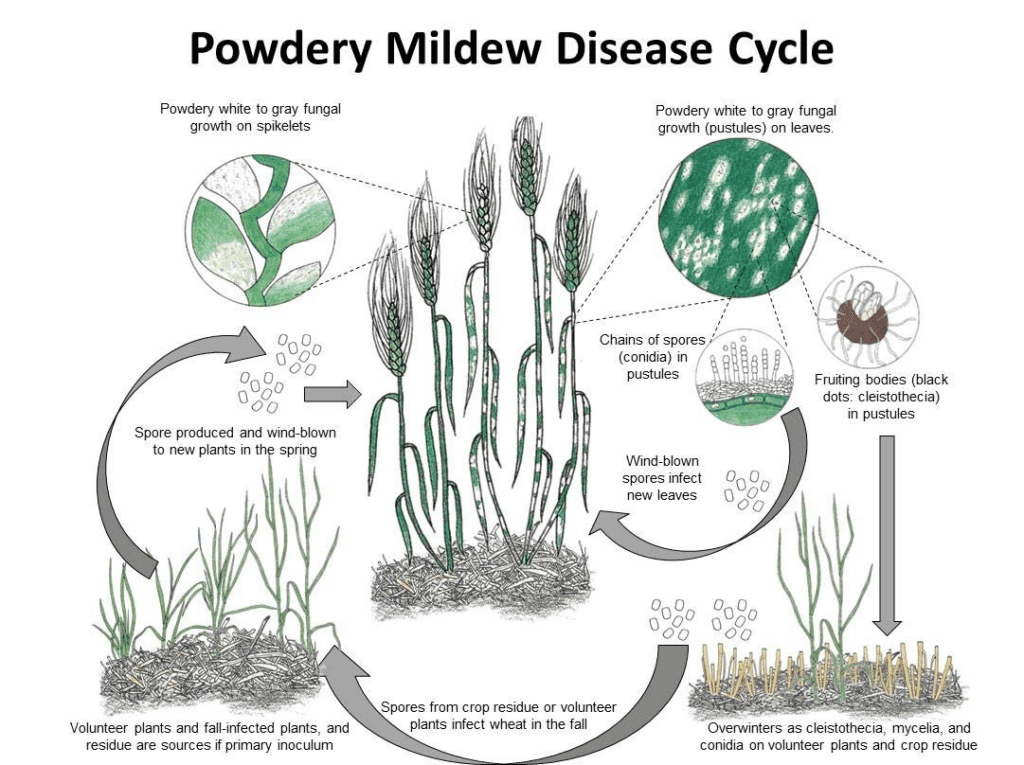
Blumeria graminis ist der Erreger des Echten Mehltaus bei Weizen und Gerste. Er kann in Form von Myzelien oder Cleistothecien überwintern. Im Frühjahr keimen die Sporen aus und infizieren die Wirtspflanzen unter kühlen und feuchten Bedingungen, ohne dass die Pflanzenoberflächen Wasser benötigen.
Der Pilz vermehrt sich sowohl ungeschlechtlich als auch geschlechtlich.
Im asexuellen Zyklus durchläuft der Erreger schnelle Zyklen der Infektion und der Konidienproduktion (ungeschlechtliche Sporen), die für die Ausbreitung der Krankheit entscheidend sind. Die Konidien werden unter günstigen Bedingungen alle 7 bis 10 Tage im Myzel gebildet. Sobald diese Konidien durch den Wind verbreitet werden, landen sie auf einem neuen Wirt, keimen und bilden Appressorien und Haustorien, um der Pflanze Nährstoffe zu entziehen. Die Konidien von Blumeria graminis können auch bei niedriger Luftfeuchtigkeit und unterschiedlichen Temperaturen keimen.
Im Sexualzyklus produziert der Pilz Cleistothecien, widerstandsfähige Strukturen, die widrige Bedingungen gut überstehen können. Cleistothecien enthalten Ascosporen (Sexualsporen), und wenn diese Sporen freigesetzt werden, werden neue Infektionen ausgelöst.
Symptome

Echter Mehltau bei Weizen und Gerste beeinträchtigt den Kornertrag, indem er die Anzahl der Ähren reduziert und die Größe und das Gewicht der Körner vermindert. Je früher die Infektion auftritt, desto größer sind die Schäden.
Gerste weist eine altersbedingte Resistenz gegen Echten Mehltau auf. Mit zunehmender Reife der Gerste können auf den Blättern statt der typischen Myzelflecken scharf begrenzte, schwarzbraune Flecken ("Teerflecken") auftreten.
Weizen ist besonders anfällig für den Echten Mehltau zwischen der Bestockung und der Milchreife, vor allem wenn die Fahnenblätter und Spelzen befallen sind. Im Vergleich zu Gerste kann Weizen jedoch frühe Infektionen besser verkraften.
Weiß-grauer Mehltau entwickelt sich auf Blättern, Stängeln und Köpfen. Der Pilzbefall tritt vor allem auf der Blattoberseite auf, kann sich aber auch auf der Unterseite entwickeln. Anfänglich erscheinen die Pusteln weiß, färben sich aber mit zunehmender Reife allmählich grau bis braun und können sich zu größeren Massen zusammenschließen, die oft von Chlorose umgeben sind. Auf der gegenüberliegenden Seite der befallenen Blätter verfärbt sich das Gewebe gelb und wird später hellbraun oder braun. Cleistothecia sind auch als kleine, runde, schwarze Punkte in älteren grauen Kolonien sichtbar. In schweren Fällen können die Blätter absterben.
Modell FieldClimate
Weizenmehltau-Modell
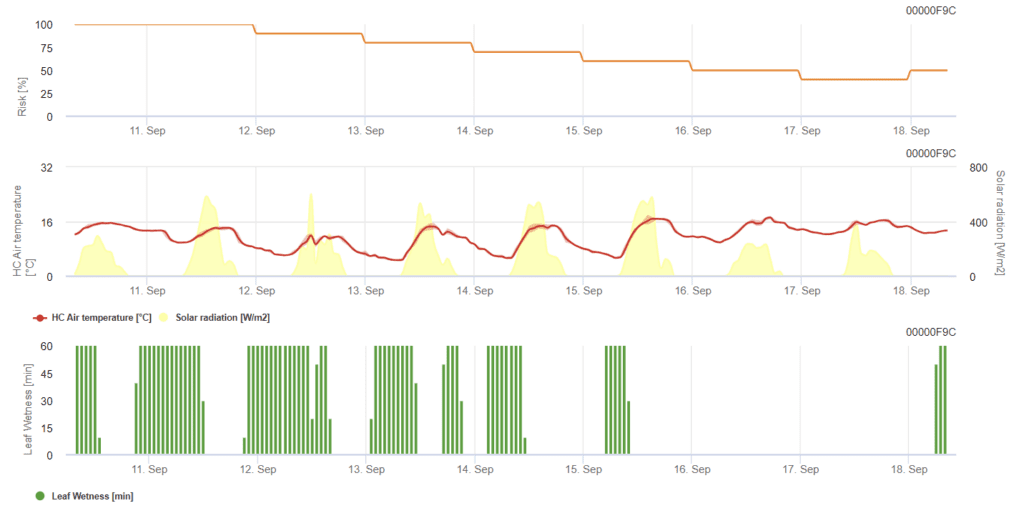
Benötigte Sensoren:
- Lufttemperatur
- Blattnässe
- Sonneneinstrahlung
Das Modell bestimmt das Mehltaustrisiko auf einer Skala von 0 (kein Befall) bis 100% (vollständiger Befall). Es ist während des BBCH-Stadiums von 21 bis 39 für Gerste und von 21 bis 75 für Weizen und Hafer relevant.
Das BBCH-Stadium ist eine Wachstumsskala zur Beschreibung der Entwicklung von Pflanzen. Die Skala hat zwei Ziffern und reicht von 00 bis 99 - 00 bezieht sich auf die Saatgutbehandlung und 99 auf die Nacherntebehandlung. Die erste Ziffer gibt das jeweilige Entwicklungsstadium an: 0 steht für die Keimung, 1 für die Blattentwicklung, 2 für die Bodenbearbeitung, 3 für die Stängelstreckung, 4 für den Austrieb, 5 für das Erscheinen und den Kopf der Blütenstände, 6 für die Blüte und die Anthese, 7 für die Fruchtentwicklung, 8 für die Reifung und 9 für die Seneszenz.
- BBCH 21: Bestockung - Beginn der Bestockung; die erste Pille ist erkennbar.
- BBCH 39: Stängelstreckung - Fahnenblattstadium; Fahnenblatt vollständig ausgerollt und Blatthäutchen gerade sichtbar.
- BBCH 75: Fruchtentwicklung - mittlere Milch; Korngehalt milchig und Körner erreichen Endgröße, sind aber noch grün.
Das Risiko steigt bei Temperaturen zwischen 12 °C und 21 °C während der meisten Stunden des Tages und bei geringer Globalstrahlung. Blattnässe, hohe Globalstrahlung und hohe Temperaturen über 32 °C verringern dagegen das Risiko.
Literatur
- Both, M., & Spanu, P. D. (2004). Blumeria graminis f. sp. hordei, ein obligater Krankheitserreger der Gerste. Annual Plant Reviews, 11, 202-218.
- Cunfer, B. M. (2002). Echter Mehltau. Brotweizen: Verbesserung und Produktion, 30, 317-330.
- Der Gräser, E. M. Krankheiten und Schädlinge des Getreides. Lancashire, P. D., Bleiholder, H., Boom, T. V. D., Langelüddeke, P., Stauss, R., Weber, E., & Witzenberger, A. (1991). Ein einheitlicher Dezimalcode für Wachstumsstadien von Kulturpflanzen und Unkräutern. Annals of Applied Biology, 119(3), 561-601. https://ohioline.osu.edu/factsheet/plpath-cer-11
Brauner Rost
Krankheitserreger
Es gibt drei wichtige Rost- und Krankheitserreger:
- Blatt-/Braunrost: Puccinia triticina
- Vorbau/ Schwarzer Rost: Puccinia graminis
- Streifen/ Gelber Rost: Puccinia striiformis
Braunrost ist die häufigste Weizenrostkrankheit. Schwarzrost wird auch als Sommerrost bezeichnet, da sich reichlich glänzende schwarze Teliosporen entwickeln. Er ist die verheerendste Rostkrankheit, die unter günstigen Bedingungen innerhalb eines Monats 50 Prozent der Verluste verursacht. Gelbrost ist eine Krankheit des Weizens in kühleren Klimazonen, die in der Regel in höheren Lagen und nördlichen Breitengraden auftritt. Sein Merkmal sind die gelb gefärbten Urediniospora. In schweren Fällen kann er ebenso große Schäden verursachen wie der Schwarzrost.
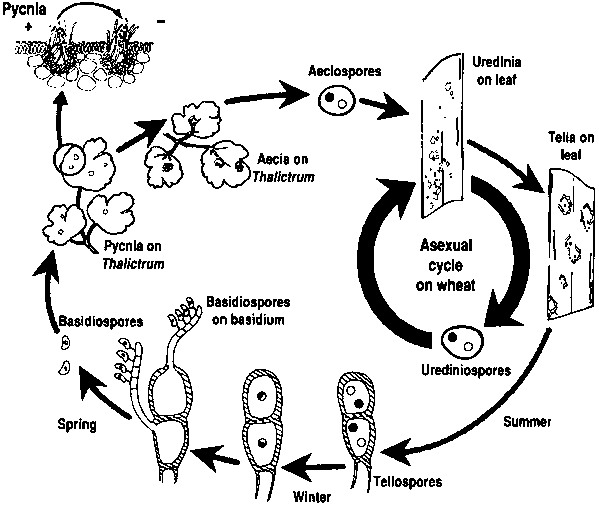
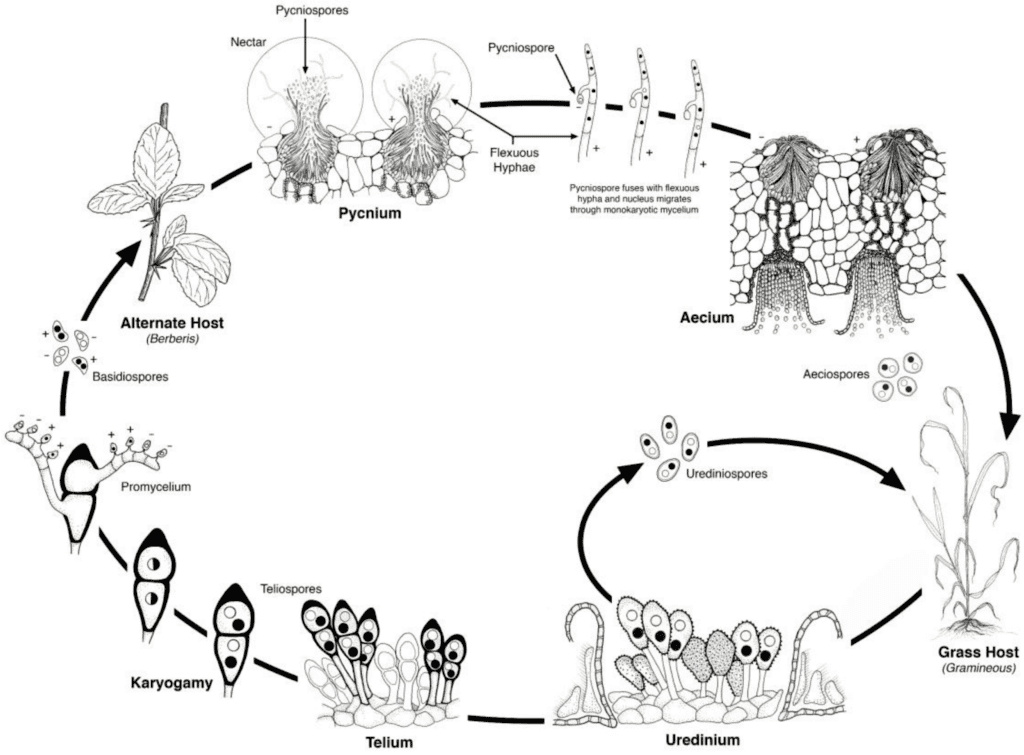
Weizenrost-Erreger durchlaufen sowohl ungeschlechtliche als auch geschlechtliche Vermehrungszyklen und benötigen zwei Wirtspflanzen - einen wirtschaftlichen Wirt und einen alternativen Wirt. Der wirtschaftliche Wirt ist Weizen, und der alternative Wirt ist in der Regel ein Unkraut oder eine einheimische Pflanze, die es dem Pilz ermöglicht, die sexuelle Phase zu durchlaufen. Puccinia striiformis ist nicht bekannt, dass sie einen alternativen Wirt hat, der aus Uredinial- und Telialstadien besteht.
Im ungeschlechtlichen Zyklus werden Urediniospora auf der Wirtspflanze produziert und können diese wiederholt infizieren, was unter günstigen Bedingungen zu einer schnellen und weit verbreiteten Infektion führt.
Der Sexualzyklus des Erregers beginnt mit der Keimung von Teliosporen, die bei Uredinialinfektionen auf der Wirtspflanze gebildet werden, und der anschließenden Meiose zur Bildung von Basidiosporen. Diese Basidiosporen werden auf einen anderen Wirt verbreitet, wo sie eine Infektion auslösen, die zur Bildung von Pyknien führt, die Pyknosporen und rezeptive Hyphen enthalten. Die Befruchtung findet statt, wenn die Pykniensporen von einem Paarungstyp über Nektar auf den anderen übertragen werden. Nach der Befruchtung entwickeln sich auf der Unterseite der Blätter des anderen Wirts Äskarienbecher, die Äskiensporen freisetzen. Diese Aeciosporen werden verbreitet und infizieren neue Wirte. Es folgt eine Infektion mit Uredinia, womit der Lebenszyklus des Erregers abgeschlossen ist.
Symptome

A) Puccinia graminis
B) Puccinia striiformis
C) Puccinia triticina
Puccinia triticina
P. triticina infiziert in erster Linie die Blattspreiten, kann aber gelegentlich auch Blattscheiden, Hüllspelzen und Grannen befallen und kleine gelbe Flecken auf der Blattoberseite bilden. Diese Flecken entwickeln sich im weiteren Verlauf der Krankheit zu orangefarbenen Pusteln, die von einem gelben Heiligenschein umgeben sind. Aus den Pusteln entstehen orangefarbene oder schwarze Sporen, die auf den Blättern sichtbar sind. Im Gegensatz zum Schwarzrost bildet er weniger Teliosporen. In einigen Fällen können überempfindliche Flecken oder Uredinia auftreten, die von chlorotischen oder nekrotischen Bereichen umgeben sind.
Puccinia graminis
P. graminis befällt vor allem Stängel, kann aber auch Blätter, Blattscheiden, Spelzen, Grannen und sogar Samen befallen. Zunächst erscheinen rötlich-braune Läsionen, und mit dem Fortschreiten der Krankheit bilden sich innerhalb der Pusteln schwarze Teliosporen. Auf den Stängeln und Blattscheiden entwickeln sich zunächst Massen von rotbraunen Urediniosporen, und es entstehen kleine chlorotische Flecken, die sich zu linearen oder rautenförmigen Pusteln entwickeln, die sich vergrößern können. Mit zunehmender Reife kommt die Produktion der Urediniosporen zum Stillstand, und es bildet sich eine Schicht schwarzer Teliosporen, die die Stängel gegen Ende der Saison schwärzlich erscheinen lassen. In schweren Fällen schwächt die Infektion die Stängel der Pflanzen, was zum Absterben führt.
Puccinia striiformis
Das charakteristische Merkmal von P. striiformis ist das Vorhandensein von geradlinigen gelben Pusteln. TJey erscheinen in schmalen, länglichen Streifen unterschiedlicher Länge, oft begleitet von Chlorose und Nekrose. Wenn die Krankheit heranreift, entwickeln sich in den Pusteln gelb-orangefarbene Sporen, und das umgebende Gewebe wird braun und trocknet aus, wodurch ein verbranntes Aussehen entsteht.
Modell FieldClimate
Puccinia-Rost-Modell
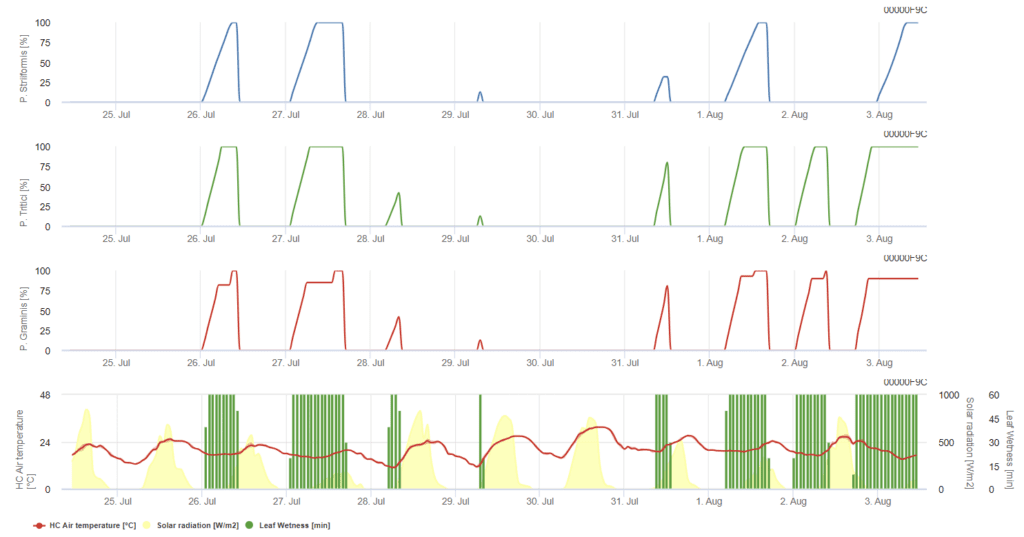
P. triticina, P. graminis, P. striiformis werden jeweils in drei verschiedenfarbigen Diagrammen dargestellt.
Puccinia triticna Infektionsmodell
Das Modell geht davon aus, dass die Infektion eine akkumulierte stündliche Temperatur von 90°C an Blattnässe in einem Lufttemperaturbereich von 5°C bis 30°C benötigt. Die Bedingungen sind vergleichbar mit P. graminis, jedoch mit einer niedrigeren Temperaturschwelle von 5°C.
Wird eine 100%-Infektion festgestellt, sollte eine kurative Pflanzenschutzmaßnahme in Betracht gezogen werden. Liegt das Risiko bei 80% und sagt die Wettervorhersage weitere Blattnässeperioden voraus, könnten Blattschutzmaßnahmen ergriffen werden.
Blattnässe bei akkumulierten stündlichen Durchschnittstemperaturen von 90°C:
- (wenn T <= 22,5°C dann ∑(Th) sonst ∑ (22,5-(Th-22,5))
- 5°C < Temp. < 30°C
Puccinia graminis-Infektionsmodell
Die Infektion erfolgt nach einigen Stunden der Blattnässe bei optimalen Temperaturbedingungen. Das Modell geht davon aus, dass die Infektion eine akkumulierte stündliche Temperatur von 80°C an Blattnässe in einem Lufttemperaturbereich von 10°C bis 35°C benötigt. Sie bevorzugt eine etwas höhere Temperatur als P. triticina und auf die Infektion muss Sonnenlicht folgen.
Wenn eine Infektion mit 100% nachgewiesen wird, waren die Bedingungen für den Pilz günstig, so dass Pflanzenschutzmaßnahmen in Betracht gezogen werden sollten.
Blattnässe für akkumulierte stündliche Durchschnittstemperaturen von 80°C, gefolgt von einer Lichtperiode (150 W/m²) für akkumulierte stündliche Durchschnittstemperaturen von 30°C:
- (wenn T <= 24°C dann ∑(Th) sonst ∑ (Th-24))
- 10°C < Temp. < 35°C
Puccinia striiformis-Infektionsmodell
Puccinia striiformis ist der Weizenrost der kühlen Klimazonen, der sein Temperaturoptimum bereits ab 15°C hat. Die Infektion erfolgt nach einigen Stunden der Blattnässe bei optimalen Temperaturbedingungen. Das Modell geht davon aus, dass eine Infektion eine akkumulierte stündliche Temperatur von 80°C Blattnässe in einem Lufttemperaturbereich von 5°C bis 20°C benötigt. In Perioden mit geringer Lichtintensität kommt es zu keinen Infektionen.
Bevor die Kurve 100% erreicht, könnten Schutzmaßnahmen ergriffen werden, während danach kurative (systemische) Schutzstrategien in Betracht gezogen werden sollten.
Blattnässe und Licht für akkumulierte stündliche Durchschnittstemperaturen für 80°C:
- (wenn T <= 15°C dann ∑(Th) sonst ∑ (Th-15))
- 5°C < Temp. < 20°C
Literatur
- Bolton, M. D., Kolmer, J. A., & Garvin, D. F. (2008). Weizenblattrost verursacht durch Puccinia triticina. Molekulare Pflanzenpathologie, 9(5), 563-575.
- Chen, X. M. (2005). Epidemiologie und Bekämpfung von Streifenrost [Puccinia striiformis f. sp. tritici] bei Weizen. Kanadische Zeitschrift für Pflanzenpathologie, 27(3), 314-337.
- Figueroa, M., Hammond-Kosack, K. E., & Solomon, P. S. (2018). Ein Überblick über Weizenkrankheiten - eine Feldperspektive. Molekulare Pflanzenpathologie, 19(6), 1523-1536.
- Guide, A. Leaf, Stem, and Stripe Rust Diseases of Wheat. Leonard, K. J., & Szabo, L. J. (2005). Stängelrost von kleinen Körnern und Gräsern, verursacht durch Puccinia graminis. Molekulare Pflanzenpathologie, 6(2), 99-111.
- Kolmer, J. (2013). Blattrost bei Weizen: Pathogenbiologie, Variation und Wirtsresistenz. Wälder, 4(1), 70-84.
- Singh, R. P., Huerta-Espino, J., Roelfs, A. P., & Curtis, B. C. (2002). Die Weizenroste. Wachstum, 2(25), 35.
Empfohlene Ausrüstung
Prüfen Sie, welcher Sensorensatz für die Überwachung potenzieller Krankheiten dieser Kultur benötigt wird.
