Impulsions modèles de maladies
brûlure d'Asochyta
Cycle de vie
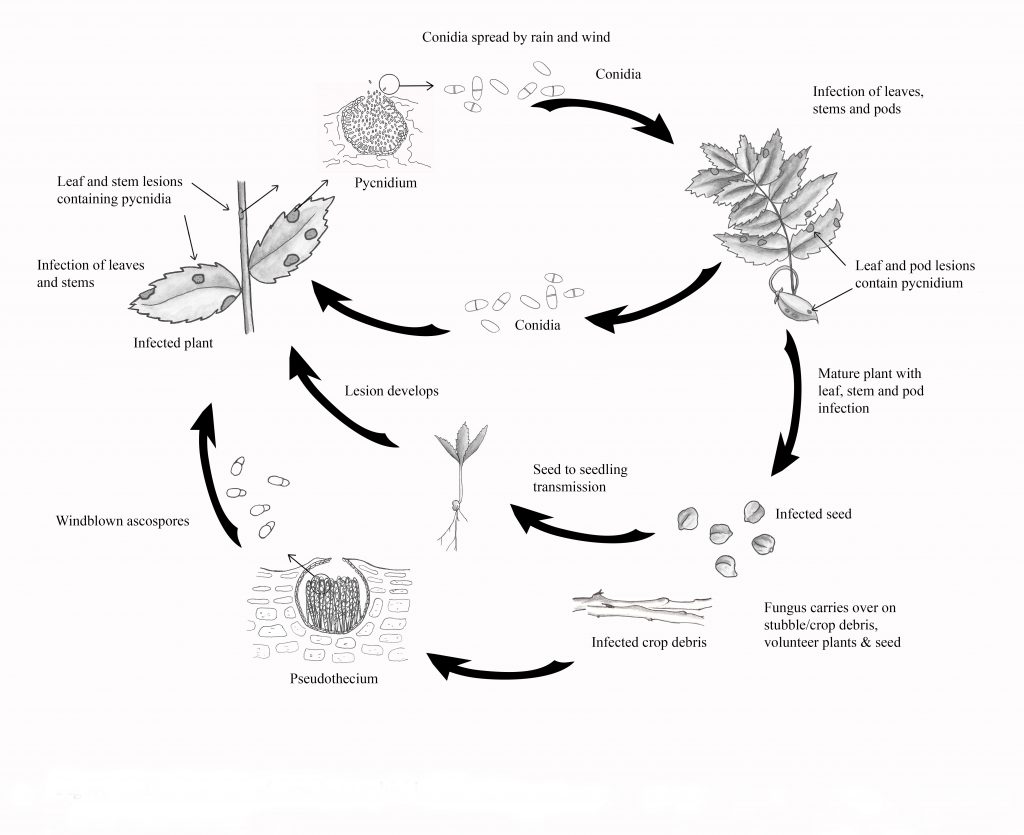
L'agent pathogène passe l'hiver sur les résidus de culture et les semences infectés. Les semences infectées peuvent jouer un rôle important dans l'introduction de l'Ascochyta Blight dans de nouvelles zones, ainsi que dans le développement précoce de la maladie, car l'agent pathogène se transmet facilement des semences aux plantules. Les spores asexuées (conidies, propagées par les éclaboussures de pluie) et les spores sexuées (ascospores, propagées par le vent) peuvent être produites sur les résidus de culture. À la fin de l'automne et au début du printemps, la reproduction sexuée produit des pseudothèces qui abritent les ascospores. Le développement des pseudothèces prend cinq à sept semaines sous une humidité adéquate et des températures modérées (près de 10°C).
Au printemps et au début de l'été, les pseudothèces matures libèrent des ascospores dans l'air, qui peuvent parcourir plusieurs kilomètres pour infecter les cultures cibles. On pense que les ascospores aéroportées sont la source initiale d'infection au printemps, bien que les conidies projetées par la pluie puissent également être impliquées. Après l'infection par les spores, les symptômes commencent à se développer dans les quatre à six jours. Les premières lésions sont de couleur beige à brun foncé, avec une marge brun foncé. Trois à six jours après la formation des lésions, des pycnides brun foncé se développent.
Les pycnides sont souvent disposées en anneaux concentriques et ne s'enlèvent pas par frottement, contrairement aux débris de tissus. Les conidies suintent des pycnides dans une masse de spores collantes et sont propagées par les éclaboussures de pluie sur les parties saines des plantes, provoquant de nouvelles infections.
La majorité des lésions pendant la saison de croissance résulte du développement rapide des pycnides et des conidies dans des conditions humides. Même de petites averses de pluie suffisent à propager les conidies aux nouveaux tissus végétaux. C'est pourquoi on parle de maladie polycyclique, ce qui signifie que de multiples cycles d'infection peuvent se produire tout au long de la saison de croissance dans des conditions d'humidité et de température adéquates (20 à 25°C).
Modèle de maladie
Nous modélisons le développement des pycnides et des conidies pendant la saison de croissance.
Le développement de la maladie de la brûlure ascochyta est optimal à des températures de 20 à 21°C (la fourchette de température est de 4°C à 34°C) et à des conditions humides (humidité relative élevée et mouillage des feuilles).
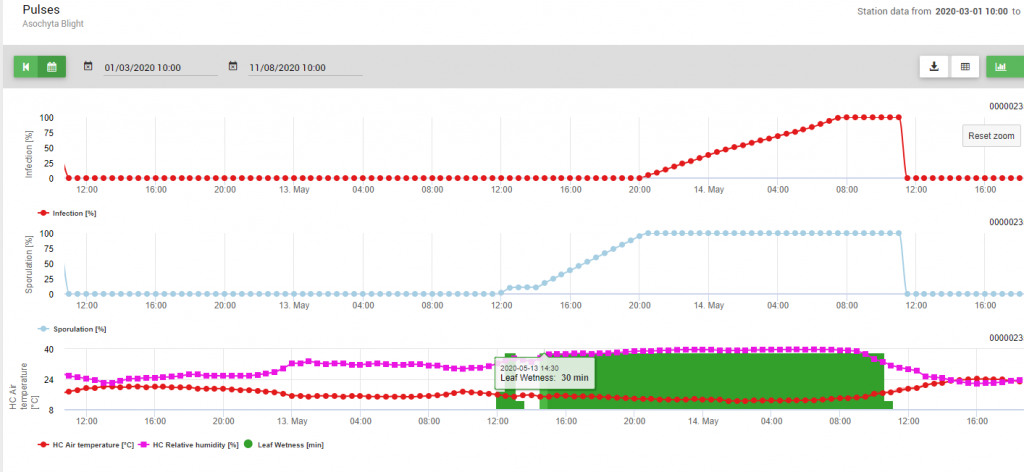
Le modèle comprend deux étapes du cycle de la maladie : 1. la sporulation (développement des pycnides, libération des conidies), qui produit de nouvelles unités infectieuses et 2. les conditions optimales pour l'infection ultérieure de ces conidies. Ainsi, pour l'infection de nouveaux tissus végétaux, les conditions optimales pour la sporulation ont d'abord été données (100%) et ensuite, la courbe d'infection a atteint 100%.
En raison des conditions optimales (humidité des feuilles, humidité relative élevée et température autour de 15°C pendant une longue période) la sporulation des pycnides a été déterminée le 13 mai à 20:00 (ligne bleue, 100%). Les conditions étaient encore optimales pour commencer la progression de l'infection (ligne rouge) et les conditions optimales pour l'infection ont été déterminées le 14 mai à 8:00 du matin (100% atteint). Ainsi, en fonction de la stratégie de protection des plantes, des mesures prophylactiques auraient dû être prises en compte déjà avant que l'infection n'ait lieu ou lors de l'utilisation de mesures curatives peu après que l'infection (100%) ait été déterminée.
La littérature :
Moisissure grise
Botrytis cinerea est un champignon nécrotrophe qui affecte de nombreuses espèces végétales, bien que ses hôtes les plus notables soient la vigne.
En viticulture, on l'appelle communément pourriture des grappes due au botrytis ; en horticulture, on l'appelle généralement moisissure grise ou pourriture grise.
Le champignon donne lieu à deux types d'infections différentes sur les raisins. La première, la pourriture grise, est le résultat de conditions constamment humides ou mouillées, et entraîne généralement la perte des grappes affectées. La seconde, la pourriture noble, se produit lorsque des conditions plus sèches succèdent à des conditions plus humides, et peut donner naissance à des vins de dessert doux et distinctifs, tels que le Sauternes ou l'Aszú de Tokaj. Le nom de l'espèce Botrytis cinerea est dérivé du latin pour "raisins comme des cendres" ; bien que poétique, le "raisins" fait référence à l'agglutination des spores fongiques sur leurs conidiophores, et "cendres" fait simplement référence à la couleur grisâtre des masses de spores. Le champignon est généralement désigné par son nom anamorphe (forme asexuée) car la phase sexuelle est rarement observée. Le téléomorphe (forme sexuelle) est un ascomycète, Botryotinia cinerea.
Biologie de B. cinerea
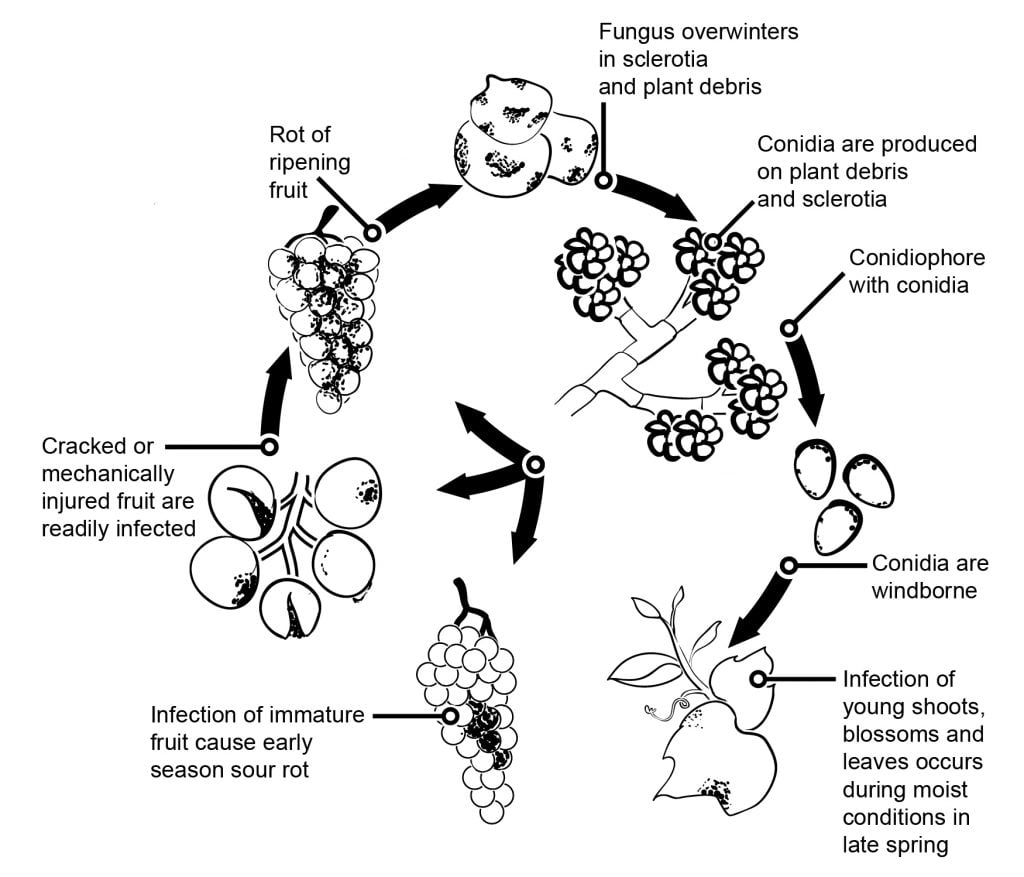
Dans les fruits et les raisins, les infections florales suivies d'une latence ont un impact important sur l'épidémiologie de la moisissure grise. On peut distinguer plusieurs voies d'infection de la fleur au fruit. Dans le raisin, les kiwis et les framboises, les infections par le stylet dans l'ovule ont été postulées. Dans l'ovule, l'agent pathogène reste latent, ce qui semble être le résultat d'une stratégie de défense de l'hôte préformatée (similaire à la teneur en resvératrol des jeunes baies de raisin). Dans le raisin, les kiwis et les fraises, les infections par les étamines, les pétales ou les sépales se sont avérées importantes. Dans le raisin, des études ont montré que B. cinerea peut infecter les étamines et se développe basipétalement pour infecter le réceptacle, puis se développe de manière systémique vers le pédicelle et les tissus vasculaires des baies.

Un projet de recherche de 6 ans dans la région du Cap a montré que les baies de raisin peuvent être infectées par le stoma et les lentilles du pédicelle et à un niveau inférieur du racheis. Les infections du pédicelle sont également possibles pendant la période de floraison. Plus tard, ce tissu augmente sa résistance contre B. cinerea infections.
D'autres voies d'infection postulent la croissance saprophyte de l'agent pathogène sur les débris floraux et l'infection ultérieure des baies lorsque la sensibilité augmente avec la maturation ou par des dégâts causés par les insectes ou la grêle sur les baies. Une autre thèse est celle de l'accumulation des conidies dans le fruit pendant l'été et l'infection des baies sensibles plus tard dans la saison. L'infection condidienne des fruits en cours de maturation est possible à partir de n'importe quelle source d'inoculum. Il est très probable qu'un faible nombre de baies infectées latentes se forment, qui présentent une sporulation extensive lorsque la sensibilité des baies augmente avec la maturité. On peut supposer que les baies deviennent sensibles à partir d'une teneur en sucre de 6%.
Dans le cas du kiwi, nous avons un impact important des conditions de cueillette sur l'apparition de B. cinerea. Les fruits cueillis avec une surface humide peuvent être infectés par B. cinerea aux microlésions provoquées par les doigts des cueilleurs.
Dans le contrôle pratique de B. cinerea nous devons séparer deux périodes d'infection importantes : la floraison et la sénescence. 1) Pendant la floraison, nous avons de jeunes fruits sensibles, où l'infection est suivie d'une période de latence. 2) Alors que l'infection sur les fruits matures (sénescents) entraînera des symptômes sans période de latence. L'importance de l'infection pendant la floraison de la vigne peut changer de saison en saison et de région en région. Pour les fruits dont la durée de vie est limitée (raisins de table, kiwis ou fraises), les symptômes apparaissent lorsqu'ils sont stockés dans des conditions réfrigérées dans des magasins ou des entrepôts. Lutte chimique contre les raisins de cuve présentant une bonne résistance aux B. cinerea pendant la floraison ne donnera aucun résultat économique. Par conséquent, toutes les conditions de risque et de probabilité d'infection, la sensibilité du fruit et la durée de conservation, les conditions de stockage doivent être prises en considération dans la décision d'une demande contre les virus de la grippe aviaire. Botrytis cinerea pendant la floraison.
Dans les fruits à noyau, l'infection par B. cinerea se produit surtout pendant la floraison. A cette époque, les traitements contre Monilina spp. sont prises en compte, ce qui a également pour effet d'infecter le Botrytis cinerea l'infection.
Modèle de B. cinerea et l'utilisation pratique
Capteurs nécessaires : Humidité des feuilles, température, humidité relative
Botrytis cinerea Botrytis cinerea est un parasite fakultatif. Il se développe également sur le matériel végétal mort. Pour cette raison, il est toujours présent dans les vignobles et les vergers. Botrytis cinerea est lié au climat humide. Pour s'infecter, il a besoin d'une humidité relative très élevée ou de la présence d'eau libre (capteur : humidité des feuilles, humidité relative). Le champignon est incapable d'infecter le matériel végétal adulte sain par les spores. L'infection a lieu sur les jeunes pousses de la vigne pendant les longues périodes humides ou sur les pousses endommagées par les tempêtes de grêle.
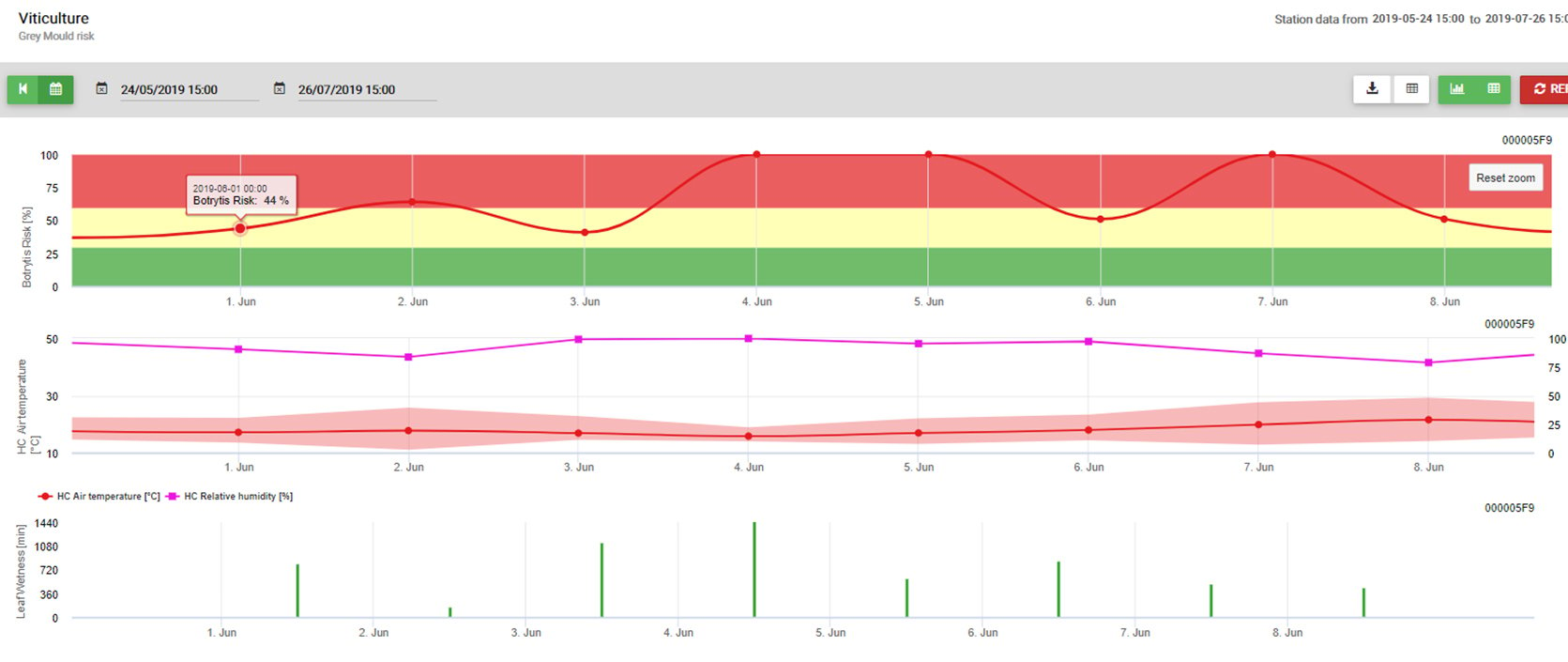
Le modèle utilise la corrélation suivante entre la durée d'humidité des feuilles et la température pour calculer le risque d'infection.
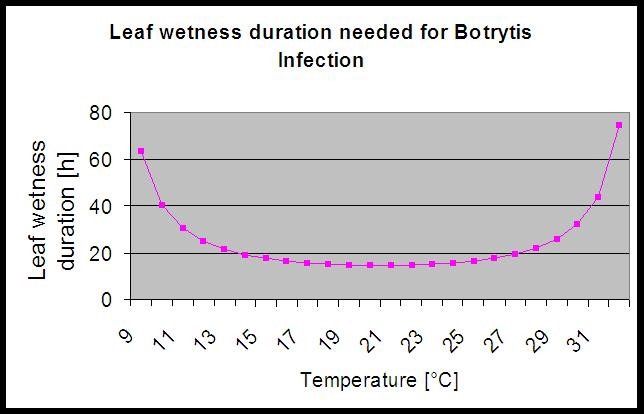
Le site Botrytis Le modèle de risque donne une valeur de risque de 0 à 100%. Cette valeur indique la pression de B. cinerea à ce moment-là. Si nous avons une valeur de 100%, cela signifie qu'il y a eu plusieurs fois une période d'humidité suffisamment longue pour infecter les tissus sensibles (nous calculons ce que l'on appelle les "points humides" (tableau entre l'humidité de la feuille, la température avec un maximum de 38400 points initialement (début de saison, qui affiche un risque de 30%). Après cette période, chaque période humide avec environ 4000 points humides (tableau) augmente le risque de 10% ou, au contraire, chaque période sèche réduit le risque de 1/5 de la valeur précédente.
Une demande contre B. cinerea dépend du fruit et de l'objectif de production.
Pourriture sclérotique
La pourriture sclérotique affecte un large éventail de plantes, en particulier les espèces non ligneuses. La pourriture sclérotique est causée par S. sclerotiorum. La pourriture sclérotique peut affecter les plantes à tous les stades de la production, y compris les semis, les plantes adultes et les produits récoltés. Les plantes dont les tissus sont sénescents ou morts sont particulièrement sensibles à l'infection.
Symptômes
La zone infectée d'une plante prend d'abord un aspect vert foncé ou brun imbibé d'eau, puis peut devenir plus pâle. Un mycélium blanc dense et cotonneux se développe généralement et la plante commence à flétrir et finit par mourir. Des structures de repos ou de survie (sclérotes) sont produites à l'extérieur sur les parties de la plante affectées et à l'intérieur dans les cavités de la moelle de la tige. Les sclérotes sont durs, noirs, de forme irrégulière, d'une taille de 2 à 4 mm pour la plupart, et difficiles à voir une fois incorporés dans le sol.
Sources et propagation des maladies
Le cycle de vie de S. sclerotiorum comprend à la fois une phase transmise par le sol et une phase transmise par l'air. Les sclérotes de S. sclerotiorum peuvent survivre dans le sol pendant dix ans ou plus. Ils germent pour produire de petits corps fructifères en forme d'entonnoir (apothécies) d'environ 1 cm de diamètre. Les apothécies produisent des spores en suspension dans l'air, qui peuvent provoquer une infection lorsqu'elles atterrissent sur une plante hôte sensible, soit par l'intermédiaire des fleurs, soit par germination directe sur les feuilles. Parfois, l'infection de la base des tiges peut se produire lorsque des brins de champignons (mycélium) se développent directement à partir des sclérotes près de la surface. De nouveaux sclérotes se développent dans les tissus végétaux infectés et, lorsque la plante meurt, ils restent à la surface du sol ou peuvent être incorporés lors d'un travail ultérieur du sol.
Conditions d'infection
Après une période de froid en hiver, les sclérotes, qui ont hiverné dans les 5 premiers centimètres du sol, germent à partir du printemps pour produire des apothécies, lorsque la température du sol est de 10°C ou plus et que le sol est humide. Les sclérotes ne germent pas dans un sol sec ou lorsque la température du sol est supérieure à 25°C. Les sclérotes enfouis à moins de 5 cm dans le sol ont moins de chances de germer. Une fois que les apothécies sont complètement formées, la libération des spores peut se produire à la lumière ou dans l'obscurité, mais elle dépend de la température et tend à atteindre un pic vers midi. Les apothécies peuvent durer environ 20 jours entre 15 et 20°C mais se ratatinent après moins de 10 jours à 25°C. Pour les herbes à fleurs, les spores qui se posent sur les pétales et les étamines germent rapidement (germination en 3-6 heures et infection en 24 heures) dans des conditions optimales de 15-25°C, d'humidité continue des feuilles et de forte humidité dans la culture. L'infection ultérieure des feuilles et des tiges dépend de la chute des pétales et de leur collage sur les feuilles. Le risque d'infection est accru si les feuilles sont humides, car les pétales collent alors davantage. Les pétales morts ou sénescents infectés fournissent des nutriments pour l'invasion du champignon dans les feuilles et les tiges. Pour les herbes non fleuries, l'infection se fait principalement par des spores transportées par l'air qui se posent directement sur les feuilles. Les spores peuvent survivre sur les feuilles pendant plusieurs semaines jusqu'à ce que les conditions favorables à l'infection des feuilles se produisent. La germination des spores et l'infection dépendent de la présence de nutriments sur les feuilles, provenant soit de blessures de la plante, soit de matériel végétal en voie de sénescence. En ce qui concerne les herbes à fleurs, les conditions optimales de germination des spores et d'infection sont de 15 à 25°C avec une humidité continue des feuilles et une forte humidité. Une fois la plante infectée, la progression rapide de la maladie est favorisée par des conditions chaudes (15-20°C) et humides dans les cultures denses.
Modèle d'infection par Sclerotinia
La germination carpogène des sclérotes est stimulée par des périodes d'humidité continue du sol. Des apothécies se forment à la surface du sol, d'où les ascospores sont libérées dans l'air. L'infection de la plupart des espèces cultivées est principalement associée aux ascospores, mais l'infection directe des tissus végétaux sains et intacts par les ascospores en germination ne se produit généralement pas. Au contraire, l'infection des tissus des feuilles et des tiges des plantes saines ne se produit que lorsque les ascospores en germination colonisent des tissus morts ou sénescents, généralement des parties de fleurs telles que les pétales abscrits, avant la formation des structures d'infection et la pénétration. La germination mycélienne des sclérotes à la surface du sol peut également entraîner la colonisation de la matière organique morte et l'infection ultérieure des plantes vivantes adjacentes. Cependant, dans certaines cultures, par exemple le tournesol, la germination mycéliogène des sclérotes peut directement initier le processus d'infection des racines et de la tige basale, entraînant le flétrissement. Le stimulus de la germination mycélienne et de l'infection du tournesol n'est pas connu mais dépend probablement des signaux nutritionnels dans la rhizosphère provenant des plantes hôtes.
Le processus d'infection
L'infection des tissus sains dépend de la formation d'un appressorium, dont la structure peut être simple ou complexe selon la surface de l'hôte. Dans la plupart des cas, la pénétration se fait directement à travers la cuticule et non par les stomates. Les appressoria se développent à partir de la ramification dichotomique terminale d'hyphes poussant sur la surface de l'hôte et consistent en un coussinet d'hyphes larges, multi-septés, courts et orientés perpendiculairement à la surface de l'hôte à laquelle ils sont attachés par du mucilage. Les appressoria complexes sont souvent appelés coussins d'infection. Bien que les premiers chercheurs aient considéré la pénétration de la cuticule comme un processus purement mécanique, des études ultrastructurales ont démontré que la digestion enzymatique de la cuticule joue également un rôle dans le processus de pénétration. On sait peu de choses sur S. sclerotiorum Cependant, le génome code pour au moins quatre enzymes de type cutinase (Hegedus, non publié). Une grande vésicule, formée à l'extrémité de l'appressorium avant la pénétration, semble être libérée dans la cuticule de l'hôte pendant la pénétration. Après la pénétration de la cuticule, une vésicule subcuticulaire se forme, à partir de laquelle de grandes hyphes se développent en éventail, recouvrant et dissolvant la paroi subcuticulaire de l'épiderme.
Infection par dégradation enzymatique des cellules épidémiques : L'acide oxalique agit en relation avec les enzymes de dégradation de la paroi cellulaire, comme la polygalacturonase (PG), pour provoquer la destruction du tissu hôte en créant un environnement propice à l'attaque par la PG de la pectine dans la lamelle moyenne. Cette attaque libère à son tour des dérivés de faible poids moléculaire qui induisent l'expression d'autres gènes de PG. En effet, l'activité PG globale est induite par la pectine ou les monosaccharides dérivés de la pectine, comme l'acide galacturonique, et est réprimée par la présence de glucose. L'examen des modèles d'expression des gènes Sspg individuels a révélé que l'interaction entre les PG et avec l'hôte au cours des différentes étapes de l'infection est finement coordonnée. (Dwayne D. Hegedus *, S. Roger Rimmer : Sclerotinia sclerotiorum : Quand ''être ou ne pas être'' un pathogène ? FEMS Microbiology Letters 251 (2005) 177-184)
La recherche de conditions climatiques propices à l'infection de S. sclerotiorum doit tenir compte de la formation des apothécies, de la sporulation, de l'infection directe par les apothécies (même si elle n'est pas très fréquente) et de l'infection à partir des mycéliums établis par dégradation enzymatique des cellules épidémiques.
Formation des apothécies et sporulation a lieu si une pluie de plus de 8 mm est suivie d'une période d'humidité relative élevée de plus de 20 heures à une température optimale de 21°C à 26°C.
Infection directe par les apothécies peut être attendue après une période d'humectation des feuilles suivie de 16 heures d'humidité relative supérieure à 90% dans des conditions optimales de 21°C à 26°C ("infection par appressoria"). Alors qu'une croissance saprophyte suivie d'une dégradation enzymatique des cellules épidermiques ("infection hydrolytique") peut être attendue sous une humidité relative légèrement inférieure à 80% pendant une période de 24 heures dans des conditions optimales de 21°C à 26°C.
La littérature :
- Lumsden, R.D. (1976) Enzymes pectolytiques de Sclerotinia sclerotiorum et leur localisation sur le haricot infecté. Can. J. Bot. 54,2630-2641.
- Tariq, V.N. et Jeffries, P. (1984) Appressorium formation by Sclerotinia sclerotiorum : scanning electron microscopy. Trans. Brit. Mycol. Soc. 82, 645-651.
- Boyle, C. (1921) Études sur la physiologie du parasitisme. VI. Infection par Sclerotinia libertiana. Ann. Bot. 35, 337-347.
- Abawi, G.S., Polach, F.J. et Molin, W.T. (1975) Infection du haricot par les ascospores de Whetzelinia sclerotiorum. Phytopathologie 65, 673-678.
- Tariq, V.N. et Jeffries, P. (1986) Ultrastructure de la pénétration de Phaseolus spp. par Sclerotinia sclerotiorum. Can. J. Bot. 64, 2909- 2915.
- Marciano, P., Di Lenna, P. et Magro, P. (1983) Oxalic acid, cell wall degrading enzymes and pH in pathogenesis and their significance in the virulence of two Sclerotinia sclerotiorum isolates on sunflower. Physiol. Plant Pathol. 22, 339-345.
- Fraissinet-Tachet, L. et Fevre, M. (1996) Regulation by galacturonic acid of ppectinolytic enzyme production by Sclerotinia sclerotiorum. Curr. Microbiol. 33, 49-53.
Utilisation pratique du modèle Sclerotinia
Le modèle d'infection de la jambe blanche indique les périodes où la formation d'apothécies est attendue. Si ces périodes coïncident avec la période de floraison du colza ou du canola, nous devons nous attendre à ce que S. sclerotiorum infections pendant une période humide. Les spores formées dans les apothécies peuvent être disponibles pendant un à plusieurs jours. L'opportunité des infections est indiquée par le calcul de la progression de l'infection pour les infections directes ou indirectes par les appressoria ou la dégradation enzymatique de la paroi cellulaire. Si la ligne de progression de l'infection atteint 100%, une infection doit être supposée. Ces infections doivent être couvertes par un traitement préventif ou un fongicide à action curative contre S. sclerotiorum doit être utilisé.
TomCast Alternaria
TOMCAST (TOMato disease foreCASTing) est un modèle informatique basé sur des données de terrain qui tente de prévoir le développement de maladies fongiques, à savoir le mildiou, la tache septorienne et l'anthracnose sur les tomates. Des enregistreurs de données placés sur le terrain enregistrent toutes les heures l'humidité et la température des feuilles. Ces données ont été analysées sur une période de 24 heures et peuvent aboutir à la formation d'une valeur de gravité de la maladie (DSV) ; essentiellement une augmentation du développement de la maladie. Au fur et à mesure que les DSV s'accumulent, la pression de la maladie continue de s'exercer sur la culture. Lorsque le nombre de DSV accumulées dépasse l'intervalle de pulvérisation, une application de fongicide est recommandée pour soulager la pression de la maladie.
TOMCAST est dérivé du modèle original F.A.S.T. (Forecasting Alternaria solani on Tomatoes) développé par les docteurs Madden, Pennypacker et MacNab ? de l'Université d'État de Pennsylvanie (PSU). Le modèle F.A.S.T. de la PSU a ensuite été modifié par le Dr Pitblado au Ridgetown College en Ontario pour devenir le modèle TOMCAST utilisé par Ohio State University Extension. Les DSV sont : Une valeur de gravité de la maladie (DSV) est l'unité de mesure donnée à un incrément spécifique de développement de la maladie (mildiou). En d'autres termes, un DSV est une représentation numérique de la rapidité ou de la lenteur avec laquelle la maladie (mildiou) s'accumule dans un champ de tomates. Le DSV est déterminé par deux facteurs ; Humidité des feuilles et température pendant les heures "d'humidité des feuilles".. Plus le nombre d'heures de mouillage des feuilles et la température augmentent, plus les DSV s'accumulent rapidement. Voir le tableau des valeurs de gravité des maladies ci-dessous.
À l'inverse, lorsqu'il y a moins d'heures de mouillage des feuilles et que la température est plus basse, les DSV s'accumulent lentement, voire pas du tout. Lorsque le nombre total de DSV accumulés dépasse une limite prédéfinie, appelée intervalle ou seuil de pulvérisation, une pulvérisation de fongicide est recommandée pour protéger le feuillage et les fruits du développement de la maladie.
Le site intervalle de pulvérisation L'intervalle de pulvérisation (qui détermine quand vous devez pulvériser) peut varier entre 15 et 20 DSV. Le DSV exact qu'un producteur doit utiliser est généralement fourni par le transformateur et dépend de la qualité du fruit. Suivre un intervalle de pulvérisation de 15 DSV est une utilisation conservatrice du système TOMCAST, ce qui signifie que vous pulvériserez plus souvent qu'un producteur qui utilise un intervalle de pulvérisation de 19 DSV avec le système TOMCAST. Le compromis se situe au niveau du nombre de pulvérisations appliquées pendant la saison et de la différence potentielle de qualité des fruits.
Des études ont été lancées à la Michigan Staate University pour tester le système de prévision des maladies, TomCast, dans le cadre de la gestion des maladies foliaires de la carotte. TomCast a été utilisé commercialement dans la production de tomates, et a récemment été adapté pour être utilisé dans la gestion des maladies de l'asperge. Les carottes de transformation 'Early Gold' ont été plantées à l'aide d'un semoir à vide de précision à la ferme de recherche sur les sols de MSU Muck, en trois rangées espacées de 18 pouces sur un lit surélevé de 50 pieds de long. Les lits de carottes étaient espacés de 64 pouces et l'espacement des graines dans le rang était de 1 pouce. Chacune des quatre répétitions de l'expérience était située dans des blocs distincts de carottes qui comprenaient 36 lits. Dix-sept planches de traitement de 20 pieds de long ont été placées au hasard en damier dans chaque réplication. Les traitements ont été appliqués à l'aide d'un pulvérisateur à dos CO2 calibré pour délivrer 50 gallons par acre de solution de pulvérisation avec des buses à jet plat 8002. Les traitements ont consisté en une application de Bravo Ultrex 82.5WDG (22.4 oz/A) sans traitement et en différents programmes d'application alternés avec Quadris 2.08SC (6.2 fl oz/A). Le programme chimique a été appliqué selon un programme calendaire de 10 jours ainsi que selon les prévisions du système TomCast de prévision des maladies. Trois différents seuils de prédiction de 15, 20 et 25 DSV ont été utilisés pour planifier les applications de fongicides. Lorsque les valeurs quotidiennes cumulées des DSV atteignaient le seuil déterminé, une pulvérisation était appliquée. Chaque régime de traitement a été initié à quatre niveaux différents de pression de la maladie (0%, trace, 5%, et 10% brûlure foliaire). Les premiers traitements ont été appliqués le 2 juillet et la dernière application de tout traitement a été faite le 21 septembre. Dix pieds de chaque rang central des blocs de pulvérisation ont été marqués avant la première application et ont été utilisés pour les évaluations hebdomadaires des maladies (voir les graphiques ci-dessous). Les rendements ont été mesurés sur la même section de dix pieds de rang en récoltant les carottes à la main, en les étêtant et en les pesant.
Cela indique que le Le premier traitement dans la carotte doit être fait dès que l'on peut trouver la première incidence de la maladie dans le champ. A partir de maintenant, cela a bien fonctionné en utilisant le modèle TomCast avec une seuil de 20 DSV accumulés depuis la dernière pulvérisation.
Fieldclimate détermine la gravité d'une infection par l'Alternaria selon deux modèles différents :
Source : Jim Jasinski, coordinateur de TOMCAST pour l'OHIO, l'INDIANA et le MICHIGAN
Équipement recommandé
Vérifiez quel jeu de capteurs est nécessaire pour surveiller les maladies potentielles de cette culture.